Лекция № 3. строение и функции белков. ферменты
Содержание:
Роль РНК и ДНК в процессе
Итак, запускает синтез белков в клетках цепочка ДНК, которая несет информацию о каком-либо конкретном белке и называется геном. Цепочка ДНК в процессе транскрипции расплетается, то есть её спираль начинает распадаться в линейную молекулу. С ДНК информация должна преобразоваться на РНК. Напротив тимина в данном процессе должен становиться аденин. Цитозин же имеет в качестве пары гуанин, точно так же, как ДНК. Напротив аденина РНК становится урацил, потому как в РНК такого нуклеотида, как тимин, не существует, он заменяется просто урациловым нуклеотидом. С гуанином соседствует цитозин. Напротив аденина становится урацил, а в паре с тимином располагается аденин. Эти молекулы РНК, которые становятся напротив, называются информационными РНК (иРНК). Они способны через поры выходить из ядра в цитоплазму и рибосомы, которые, собственно, и выполняют функцию синтеза белков в клетках.
Методы изучения
Сегодня исследование белковых соединений продолжается в современных лабораториях.
Популярные методы изучения:
- Метод клеточной и молекулярной биологии используется с целью фиксирования локализации молекул в клетках, наблюдения за синтезом веществ. Для стимулирования реакции используются антитела. Наблюдение проводится посредством микроскопа. На предметное стекло помещается подготовленный белок и антитела, проводится эксперимент, результаты фиксируются.
- Биохимический метод предполагает изучение чистого белка, избавленного от дополнительных компонентов. Для дальнейшего изучения используют центрифугирование, высаливание, электрофокусирование.
- Протеомика — наука, изучающая совокупность белковых соединений в составе одной клетки. Для исследования используются специальные приборы, соединения, белковые микрочипы, позволяющие изучать сразу несколько молекул в клетке.
Благодаря новейшим современным методикам возможно прогрессирование науки в области исследования живых клеток и их составляющих.

Бизнес и финансы
БанкиБогатство и благосостояниеКоррупция(Преступность)МаркетингМенеджментИнвестицииЦенные бумагиУправлениеОткрытые акционерные обществаПроектыДокументыЦенные бумаги — контрольЦенные бумаги — оценкиОблигацииДолгиВалютаНедвижимость(Аренда)ПрофессииРаботаТорговляУслугиФинансыСтрахованиеБюджетФинансовые услугиКредитыКомпанииГосударственные предприятияЭкономикаМакроэкономикаМикроэкономикаНалогиАудитМеталлургияНефтьСельское хозяйствоЭнергетикаАрхитектураИнтерьерПолы и перекрытияПроцесс строительстваСтроительные материалыТеплоизоляцияЭкстерьерОрганизация и управление производством
Обеспечивает энергией
Белки могут снабжать ваш организм энергией.
Белок содержит четыре калории на грамм – такое же количество энергии, которое обеспечивают углеводы. Жиры обеспечивают организм наибольшим количеством энергии – девять калорий на грамм.
Тем не менее последнее, что ваш организм хочет использовать для производства энергии, это белок, так как это ценное питательное вещество широко используется во всем вашем теле.
Углеводы и жиры намного лучше подходят для обеспечения организма энергией, так как ваше тело имеет резервы для использования его в качестве топлива. Более того, они метаболизируются более эффективно по сравнению с белком ().
Фактически, белок снабжает ваш организм очень незначительным количеством энергии при нормальных обстоятельствах.
Однако в состоянии голода (18-48 часов без приема пищи) ваш организм начинает расщеплять скелетные мышцы, чтобы аминокислоты могли снабжать вас энергией (, ).
Ваше тело также использует аминокислоты из расщепленных скелетных мышц, если уровень хранимых углеводов низок. Это может произойти после истощающих физических нагрузок или если вы не потребляете достаточно калорий в целом ().
Аминокислотный состав белков
Белки — непериодические полимеры, мономерами которых являются α-аминокислоты. Обычно в качестве мономеров белков называют 20 видов α-аминокислот, хотя в клетках и тканях их обнаружено свыше 170.
В зависимости от того, могут ли аминокислоты синтезироваться в организме человека и других животных, различают: заменимые аминокислоты — могут синтезироваться; незаменимые аминокислоты — не могут синтезироваться. Незаменимые аминокислоты должны поступать в организм вместе с пищей. Растения синтезируют все виды аминокислот.
В зависимости от аминокислотного состава, белки бывают: полноценными — содержат весь набор аминокислот; неполноценными — какие-то аминокислоты в их составе отсутствуют. Если белки состоят только из аминокислот, их называют простыми. Если белки содержат помимо аминокислот еще и неаминокислотный компонент (простетическую группу), их называют сложными. Простетическая группа может быть представлена металлами (металлопротеины), углеводами (гликопротеины), липидами (липопротеины), нуклеиновыми кислотами (нуклеопротеины).
Все аминокислоты содержат: 1) карбоксильную группу (–СООН), 2) аминогруппу (–NH2), 3) радикал или R-группу (остальная часть молекулы). Строение радикала у разных видов аминокислот — различное. В зависимости от количества аминогрупп и карбоксильных групп, входящих в состав аминокислот, различают: нейтральные аминокислоты, имеющие одну карбоксильную группу и одну аминогруппу; основные аминокислоты, имеющие более одной аминогруппы; кислые аминокислоты, имеющие более одной карбоксильной группы.
Аминокислоты являются амфотерными соединениями, так как в растворе они могут выступать как в роли кислот, так и оснований. В водных растворах аминокислоты существуют в разных ионных формах.
Недостаток белка в организме
Недостаток белка в организме наблюдается при длительном нарушении баланса между поступлением и распадом белка в организме, когда процесс распада начинает преобладать. Ее причина заключается в малом потреблении белка с пищей или в преимущественном потреблении белков низкой биологической ценности, которые характеризуются дефицитом незаменимых аминокислот. При этом рацион может удовлетворять потребность организма в энергии за счет углеводов и жиров. Однако энергетическая недостаточность усугубляет нехватку белков: белки начинают расходоваться на энергетические затраты организма, а усвоение поступающего с пищей белка ухудшается.
При нарушении принципов рационального питания, что может быть вызвано неблагоприятными социально-экономическими факторами или увлечением физиологически не обоснованными диетами, возникает так называемая алиментарная белковая недостаточность. Но чаще белковая недостаточность обусловлена различными заболеваниями. Переваривание и всасывание белка нередко нарушаются при болезнях органов пищеварения, особенно поджелудочной железы и кишечника. Повышенный расход или потери белка наблюдаются при активном туберкулезе, инфекционных заболеваниях, болезнях почек, тяжелых травмах и операциях, обширных ожогах, злокачественных новообразованиях, массивных кровопотерях и т. д.
При болезнях печени или почек к данному состоянию могут привести излишне продолжительные малобелковые диеты.
Здоровому взрослому человеку в сутки нужно потреблять около 80-90 граммов белка, половина из которых должна приходиться на долю: животных продуктов.
Белковая недостаточность способствует ухудшению работы пищеварительной системы (особенно печени и поджелудочной железы), эндокринной, кроветворной, иммунной и других систем организма, атрофии мышц. Организм начинает менее эффективно усваивать другие пищевые вещества, что ведет к появлению соответствующих дефицитных состояний, например гиповитаминозов. Снижаются работоспособность и сопротивляемость инфекциям, замедляется выздоровление при различных заболеваниях, в частности заживление ран после операций и травм.
Белки-рецепторы
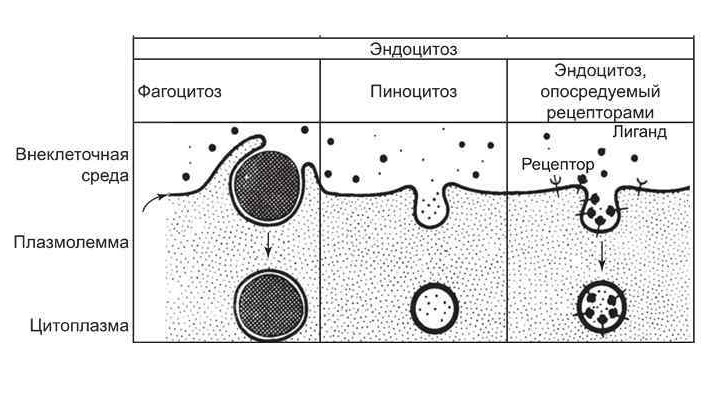
К белкам с регуляторной функцией можно отнести также белки-рецепторы. Мембранные белки-рецепторы передают сигнал с поверхности клетки внутрь, преобразовывая его. Они регулируют функции клеток за счет связывания с лигандом, который «сел» на этот рецептор снаружи клетки; в результате активируется другой белок внутри клетки.
Большинство гормонов действуют на клетку, только если на её мембране есть определенный рецептор — другой белок или гликопротеид. Например, β2- адренорецептор находится на мембране клеток печени. При стрессе молекула адреналина связывается с β2- адренорецептором и активирует его. Далее активированный рецептор активирует G-белок , который присоединяет ГТФ . После многих промежуточных этапов передачи сигнала происходит фосфоролиз гликогена. Рецептор осуществил самую первую операцию по передаче сигнала, ведущего к расщеплению гликогена . Без него не было бы последующих реакций внутри клетки.
Функции белков.
Белки в клетке выполняют важные и многообразные функции. Прежде всего они выполняют строительную функцию
. Из белков состоят мембраны клеток и клеточных органоидов. У высших животных в основном из белков состоят стенки кровеносных сосудов, сухожилия, хрящи и т. д.
Громадное значение имеет каталитическая функция белков
. Из курса химии вам известно, что скорость химических реакций зависит от свойств реагирующих веществ, от их концентрации и температуры, при которой идет реакция. Химическая активность веществ в живой клетке, как правило, невелика. Концентрации их в клетке большей частью незначительны. Температура клеточной среды невысокая. Таким образом, реакции в клетке должны были бы протекать очень медленно. Между тем реакции в клетке идут с большими скоростями. Это достигается благодаря наличию в клетке катализаторов. Клеточные катализаторы называются ферментами. Каталитическая активность ферментов исключительно велика. Они ускоряют реакции в десятки, сотни миллионов раз. По химической структуре ферменты — белки. В большинстве случаев ферменты катализируют превращения веществ, размеры молекул которых по сравнению с размерами макромолекулы фермента очень малы. Например, фермент ката-лаза имеет молекулярную массу 250000, а пероксид водорода (Н 2 О 2), распад которого катализирует каталаза, всего 34. Такое соотношение между размерами фермента и веществом, на которое он действует, наводит на мысль, что каталитическая активность фермента определяется не всей его молекулой, а только небольшим ее участком — активным центром фермента. Как известно, реакция между веществами происходит при условии тесного сближения их молекул. Возможность сближения фермента и вещества происходит благодаря геометрическому соответствию структур активного центра фермента и молекулы вещества. Они подходят друг к другу, «как ключ к замку». При денатурации фермента его каталитическая активность исчезает, так как нарушается структура активного центра.
Почти каждая химическая реакция в клетке катализируется особым ферментом. Число различных реакций, протекающих в клетке, достигает нескольких тысяч. Соответственно в клетке обнаружено несколько тысяч разных ферментов.
Кроме строительной и каталитической функций, важна сигнальная функция белков
. В поверхностную мембрану клетки встроены молекулы белков, способных изменять свою третичную структуру в ответ на действие факторов внешней среды. Так происходит прием сигналов из внешней среды и передача команд в клетку.
Белкам присуща также двигательная функция
. Движение — одно из проявлений жизненной активности. Все виды движения, к которым способны клетки у высших животных, в том числе и сокращение мышц, а также мерцание ресничек у простейших, движения жгутиков, выполняют особые сократительные белки.
Белки выполняют также транспортную функцию
. Они способны присоединять различные вещества и переносить их из одного места клетки в другое. Белок крови гемоглобин присоединяет кислород и разносит его ко всем тканям и органам тела.
Большое значение имеет защитная функция белков
. При введении чужеродных белков или клеток в организм в нем происходит выработка особых белков, которые связывают и обезвреживают чужеродные клетки и вещества.
Следует отметить, наконец, энергетическую функцию белков
. Белки распадаются в клетке до аминокислот. Часть аминокислот используется для синтеза белков, часть же подвергается глубокому расщеплению, в ходе которого освобождается энергия. При полном расщеплении 1 г белка освобождается 17,6 кДж.
О громадном значении белков для жизни догадывались давно. Сто лет назад Ф. Энгельс писал, что «жизнь есть форма существования белковых тел». Эта фраза стала крылатой, в ней подчеркивается решающее значение белков для жизни. Данные современной биологии полностью подтверждают этот вывод.
1 уровень
Он представлен последовательностью аминокислотных остатков полипептидной цепи. Как правило, его описывают с использованием одно- либо трехбуквенных обозначений. Первичная структура белков отличается устойчивыми сочетаниями аминокислотных остатков. Они выполняют определенные задачи. Такие «консервативные мотивы» остаются сохраненными в ходе видовой эволюции. По ним достаточно часто можно предсказывать задачу неизвестного протеина. Оценивая степень сходства (гомологии) в аминокислотных цепях от различных организмов, можно определять эволюционное расстояние, образующееся между таксонами, которые составляют эти организмы. Первичная структура белков определяется методом секвенирования либо по исходному комплексу его мРНК с использованием таблицы генетического кода.
Почему нам важно употреблять белки в пищу?
Белки состоят из аминокислот. Именно они и представляют ценность для нашего организма. Различные белки имеют разный состав. Какие-то из них более важны для рациона человека, какие-то – менее.
Из белков, содержащихся в пище, мы можем получить 20 аминокислот, 8 из которых являются незаменимыми. Последние не синтезируются нашим организмом, их источником выступают исключительно продукты питания. Остальные 12 производятся человеком самостоятельно из белков при употреблении их в пищу. Недостаток незаменимых аминокислот нарушает белковый обмен. В этом случае происходят сбои в работе всех органов и систем. Чтобы этого не допустить, необходимо следить за тем, чтобы в рационе ежедневно присутствовали все 8 незаменимых аминокислот.
Источники незаменимых аминокислот
Недавние исследования, проведённые шведскими и немецкими учёными, доказали, что белки, содержащие все 8 незаменимых аминокислот, могут быть получены из продуктов питания растительного происхождения. Полноценные вещества человек может приобрести из большинства фруктов и овощей, злаков, бобовых и орехов. Кроме того, растительная пища содержит все необходимые витамины и минеральные вещества, создаёт в кишечнике здоровую микрофлору и мягко очищает организм. Люди, придерживающиеся растительного рациона питания, не только не испытывают недостатка в белках, но и обладают крепким здоровьем и отличным самочувствием.
Сочетание всех незаменимых аминокислот вы найдёте в следующих продуктах (сверху – наиболее богатые белками):
- горох и фасоль;
- гречневая, манная, овсяная, пшённая крупа;
- кукурузная, перловая крупы, рис, хлеб;
- цветная капуста, картофель;
- остальные овощи, фрукты и ягоды.
Пространственная организация белковых молекул
Выполнение белками определенных специфических функций зависит от пространственной конфигурации их молекул, кроме того, клетке энергетически невыгодно держать белки в развернутой форме, в виде цепочки, поэтому полипептидные цепи подвергаются укладке, приобретая определенную трехмерную структуру, или конформацию. Выделяют 4 уровня пространственной организации белков.
Первичная структура белка — последовательность расположения аминокислотных остатков в полипептидной цепи, составляющей молекулу белка. Связь между аминокислотами — пептидная.
Если молекула белка состоит всего из 10 аминокислотных остатков, то число теоретически возможных вариантов белковых молекул, отличающихся порядком чередования аминокислот, — 1020. Имея 20 аминокислот, можно составить из них еще большее количество разнообразных комбинаций. В организме человека обнаружено порядка десяти тысяч различных белков, которые отличаются как друг от друга, так и от белков других организмов.
Именно первичная структура белковой молекулы определяет свойства молекул белка и ее пространственную конфигурацию. Замена всего лишь одной аминокислоты на другую в полипептидной цепочке приводит к изменению свойств и функций белка. Например, замена в β-субъединице гемоглобина шестой глутаминовой аминокислоты на валин приводит к тому, что молекула гемоглобина в целом не может выполнять свою основную функцию — транспорт кислорода; в таких случаях у человека развивается заболевание — серповидноклеточная анемия.
Вторичная структура — упорядоченное свертывание полипептидной цепи в спираль (имеет вид растянутой пружины). Витки спирали укрепляются водородными связями, возникающими между карбоксильными группами и аминогруппами. Практически все СО- и NН-группы принимают участие в образовании водородных связей. Они слабее пептидных, но, повторяясь многократно, придают данной конфигурации устойчивость и жесткость. На уровне вторичной структуры существуют белки: фиброин (шелк, паутина), кератин (волосы, ногти), коллаген (сухожилия).
Третичная структура — укладка полипептидных цепей в глобулы, возникающая в результате возникновения химических связей (водородных, ионных, дисульфидных) и установления гидрофобных взаимодействий между радикалами аминокислотных остатков. Основную роль в образовании третичной структуры играют гидрофильно-гидрофобные взаимодействия. В водных растворах гидрофобные радикалы стремятся спрятаться от воды, группируясь внутри глобулы, в то время как гидрофильные радикалы в результате гидратации (взаимодействия с диполями воды) стремятся оказаться на поверхности молекулы. У некоторых белков третичная структура стабилизируется дисульфидными ковалентными связями, возникающими между атомами серы двух остатков цистеина. На уровне третичной структуры существуют ферменты, антитела, некоторые гормоны.
Четвертичная структура характерна для сложных белков, молекулы которых образованы двумя и более глобулами. Субъединицы удерживаются в молекуле благодаря ионным, гидрофобным и электростатическим взаимодействиям. Иногда при образовании четвертичной структуры между субъединицами возникают дисульфидные связи. Наиболее изученным белком, имеющим четвертичную структуру, является гемоглобин. Он образован двумя α-субъединицами (141 аминокислотный остаток) и двумя β-субъединицами (146 аминокислотных остатков). С каждой субъединицей связана молекула гема, содержащая железо.
Если по каким-либо причинам пространственная конформация белков отклоняется от нормальной, белок не может выполнять свои функции. Например, причиной «коровьего бешенства» (губкообразной энцефалопатии) является аномальная конформация прионов — поверхностных белков нервных клеток.
Виды белков
Виды белков бывают следующие:
- Белки куриных яиц. Они усваиваются лучше всего и считаются эталонными. Всем известно, что яйца включают белок, который почти на 100 % состоит из альбумина, и желток.
- Казеин. При попадании в желудок вещество превращается в сгусток, который долгое время переваривается. Это обеспечивает невысокую скорость расщепления белка, что провоцирует стабильное снабжение организма аминокислотами.
- Белки молочной сыворотки. Такие компоненты расщепляются быстрее всего. Уровень аминокислот и пептидов в крови увеличивается уже в течение 1 часа после употребления таких продуктов. При этом кислотообразующая функция желудка остается неизменной.
- Соевые белки. Такие вещества имеют сбалансированный состав важных аминокислот. После употребления подобных продуктов снижается содержание холестерина. Потому такую пищу стоит есть людям с лишним весом. При этом главным минусом соевых белков считается наличие ингибитора пищеварительного фермента трипсина.
- Растительные белки. Такие вещества усваиваются человеческим организмом достаточно плохо. Их клетки обладают толстыми оболочками, которые не поддаются влиянию пищеварительного сока. Также проблемы с усвоением обусловлены наличием ингибиторов пищеварительных ферментов в отдельных растениях.
- Рыбный белок. Изолят рыбного белка достаточно медленно расщепляется до состояния аминокислот.
Недостаток белков
Белковая недостаточность может развиться по следующим причинам:
- Основная причина – недостаточное поступление белков с пищей. Это может случиться, если человек сидит на диете, если его рацион питания содержит их в небольшом количестве.
- Заболевания, препятствующие поступлению пищи: перекрытие пищевода, воспаление слизистой оболочки рта.
- Заболевания ЖКТ и их последствия, из-за которых затруднено всасывание питательных веществ.
- Белки расходуются при ожогах большой площади тела, серьёзных ранах, онкологических заболеваниях.
- Проблемы с гормонами.
Симптомы, которые могут указывать на возникновение белковой недостаточности:
- уменьшение массы тела;
- бледность, сухость кожи, при тяжёлой недостаточности она становится дряблой и вялой;
- частые диареи;
- снижение либидо, отсутствие менструаций у женщин;
- раздражительность, невнимательность, постоянная усталость, плохой аппетит;
- , человека преследуют инфекционные заболевания.
Лёгкая степень нехватки белка устраняется пересмотром рациона и включением в него всех необходимых аминокислот из расчёта на идеальный вес пациента.
Внутриклеточные регуляторные белки
Белки регулируют процессы, происходящие внутри клеток, при помощи нескольких механизмов:
- взаимодействия с молекулами ДНК (транскрипционные факторы);
- при помощи фосфорилирования (протеинкиназы) или дефосфорилирования (протеинфосфатазы) других белков;
- при помощи взаимодействия с рибосомой или молекулами РНК (факторы регуляции трансляции);
- воздействия на процесс удаления интронов (факторы регуляции сплайсинга);
- влияния на скорость распада других белков (убиквитины и др.).
Белки-регуляторы транскрипции
Транскрипционный фактор
— это белок, который, попадая в ядро , регулирует транскрипцию ДНК, то есть считывание информации с ДНК на мРНК (синтез мРНК по матрице ДНК). Некоторые транскрипционные факторы изменяют структуру хроматина, делая его более доступным для РНК-полимераз. Существуют различные вспомогательные транскрипционные факторы, которые создают нужную конформацию ДНК для последующего действия других транскрипционных факторов. Еще одна группа транскрипционных факторов — это те факторы, которые не связываются непосредственно с молекулами ДНК, а объединяются в более сложные комплексы с помощью белок-белковых взаимодействий.
Факторы регуляции трансляции
Трансляция
— синтез полипептидных цепей белков по матрице мРНК, выполняемый рибосомами. Регуляция трансляции может осуществляться несколькими способами, в том числе и с помощью белков-репрессоров, которые, связываются с мРНК. Известно много случаев, когда репрессором является белок, который кодируется этой мРНК. В этом случае происходит регуляция по типу обратной связи (примером этого может служить репрессия синтеза фермента треонил-тРНК-синтетазы).
Факторы регуляции сплайсинга
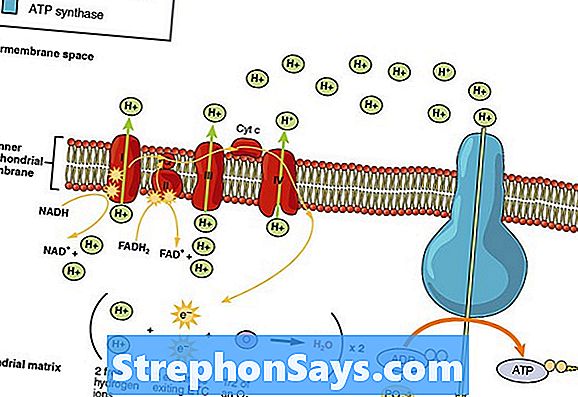
Внутри генов эукариот есть участки, не кодирующие аминокислот. Эти участки называются интронами . Они сначала переписываются на пре-мРНК при транскрипции, но затем вырезаются особым ферментом. Этот процесс удаления интронов, а затем последующее сшивание концов оставшихся участков называют сплайсингом (сшивание, сращивание). Сплайсинг осуществляется с помощью небольших РНК, обычно связанных с белками, которые называются факторами регуляции сплайсинга. В сплайсинге принимают участие белки, обладающие ферментативной активностью. Они придают пре-мРНК нужную конформацию. Для сборки комплекса (сплайсосомы) необходимо потребление энергии в виде расщепляемых молекул АТФ, поэтому в составе этого комплекса есть белки, обладающие АТФ-азной активностью.
Существует альтернативный сплайсинг . Особенности сплайсинга определяются белками, способными связываться с молекулой РНК в областях интронов или участках на границе экзон-интрон. Эти белки могут препятствовать удалению одних интронов и в то же время способствовать вырезанию других. Направленная регуляция сплайсинга может иметь значительные биологические последствия. Например, у плодовой мушки
Существуют
несколько видов защитных функций белков:
Физическая
защита. В ней принимает участие коллаген —
белок, образующий основу межклеточного
вещества соединительных тканей (в том
числе костей, хряща, сухожилий и глубоких
слоёв кожи (дермы)); кератин,
составляющий основу роговых щитков,
волос, перьев, рогов и др. производныхэпидермиса.
Обычно такие белки рассматривают как
белки со структурной функцией. Примерами
этой группы белков служат фибриногены итромбины ,
участвующие в свёртывании крови.
Химическая
защита. Связывание токсинов белковыми
молекулами может обеспечивать их
детоксикацию. Особенно важную роль в
детоксикации у человека играют ферменты печени,
расщепляющие яды или переводящие их в
растворимую форму, что способствует
их быстрому выведению из организма .
Иммунная
защита. Белки, входящие в состав крови и
других биологических жидкостей,
участвуют в защитном ответе организма
как на повреждение, так и на атаку патогенов.
Белки системы
комплемента и антитела (иммуноглобулины)
относятся к белкам второй группы; они
нейтрализуют бактерии, вирусы или
чужеродные белки. Антитела, входящие
в состав адаптативной
иммунной системы,
присоединяются к чужеродным для данного
организма веществам, антигенам,
и тем самым нейтрализуют их, направляя
к местам уничтожения. Антитела
могутсекретироваться в
межклеточное пространство или
закрепляться в мембранах
специализированных В-лимфоцитов,
которые называютсяплазмоцитами .
В то время как ферменты имеют ограниченное
сродство к субстрату, поскольку слишком
сильное присоединение к субстрату
может мешать протеканию катализируемой
реакции, стойкость присоединения
антител к антигену ничем не ограничена .
3. Внутриклеточные регуляторные белки
Белки регулируют процессы, происходящие внутри клеток, при помощи нескольких механизмов:
- взаимодействия с молекулами ДНК (транскрипционные факторы)
- при помощи фосфорилирования (протеинкиназы) или дефосфорилирования (протеинфосфатазы) других белков
- при помощи взаимодействия с рибосомой или молекулами РНК (факторы регуляции трансляции)
- воздействия на процесс удаления интронов (факторы регуляции сплайсинга)
- влияния на скорость распада других белков (убиквитины и др.)
3.1. Белки-регуляторы транскрипции
Транскрипционный фактор
— это белок, который, попадая в ядро, регулирует транскрипцию ДНК, то есть считывание информации с ДНК на мРНК (синтез мРНК по матрице ДНК). Некоторые транскрипционные факторы изменяют структуру хроматина, делая его более доступным для РНК-полимераз. Существуют различные вспомогательные транскрипционные факторы, которые создают нужную конформацию ДНК для последующего действия других транскрипционных факторов. Еще одна группа транскрипционных факторов — это те факторы, которые не связываются непосредственно с молекулами ДНК, а объединяются в более сложные комплексы с помощью белок-белковых взаимодействий.
3.2. Факторы регуляции трансляции
Трансляция
— синтез полипептидных цепей белков по матрице мРНК, выполняемый рибосомами. Регуляция трансляции может осуществляться несколькими способами, в том числе и с помощью белков-репрессоров, которые, связываются с мРНК. Известно много случаев, когда репрессором является белок, который кодируется этой мРНК. В этом случае происходит регуляция по типу обратной связи (примером этого может служить репрессия синтеза фермента треонил-тРНК-синтетазы).
3.3. Факторы регуляции сплайсинга
Внутри генов эукариот есть участки, не кодирующие аминокислот. Эти участки называются интронами. Они сначала переписываются на пре-мРНК при транскрипции, но затем вырезаются особым ферментом. Этот процесс удаления интронов, а затем последующее сшивание концов оставшихся участков называют сплайсингом (сшивание, сращивание). Сплайсинг осуществляется с помощью небольших РНК, обычно связанных с белками, которые называются факторами регуляции сплайсинга. В сплайсинге принимают участие белки, обладающие ферментативной активностью. Они придают пре-мРНК нужную конформацию. Для сборки комплекса(сплайсосомы) необходимо потребление энергии в виде расщепляемых молекул АТФ, поэтому в составе этого комплекса есть белки, обладающие АТФ-азной активностью.
Существует альтернативный сплайсинг. Особенности сплайсинга определяются белками, способными связываться с молекулой РНК в областях интронов или участках на границе экзон-интрон. Эти белки могут препятствовать удалению одних интронов и в то же время способствовать вырезанию других. Направленная регуляция сплайсинга может иметь значительные биологические последствия. Например, у плодовой мушки дрозофилы альтернативный сплайсинг лежит в основе механизма определения пола.
3.4. Протеинкиназы и протеинфосфатазы
Важнейшую роль в регуляции внутриклеточных процессов играют протеинкиназы — ферменты, которые активируют или подавляют активность других белков путем присоединения к ним фосфатных групп.
Протеинкиназы регулируют активность других белков путем фосфолирования — присоединения остатков фосфорной кислоты к остаткам аминокислот, имеющих гидроксильные группы. При фосфорилировании обычно изменяется функционирование данного белка, например, ферментативная активность, а также положение белка в клетке.
Существуют также протеинфосфатазы — белки,которые отщепляют фосфатные группы. Протеинкиназы и протеинфосфатазы регулируют обмен веществ, а также передачу сигналов внутри клетки. Фосфорилирование и дефосфорилирования белков — один из главным механизмов регуляции большинства внутриклеточных процессов.
Цикл активации G-белка под действием рецептора.
Синхронизация выполнена 18.07.11 07:59:14
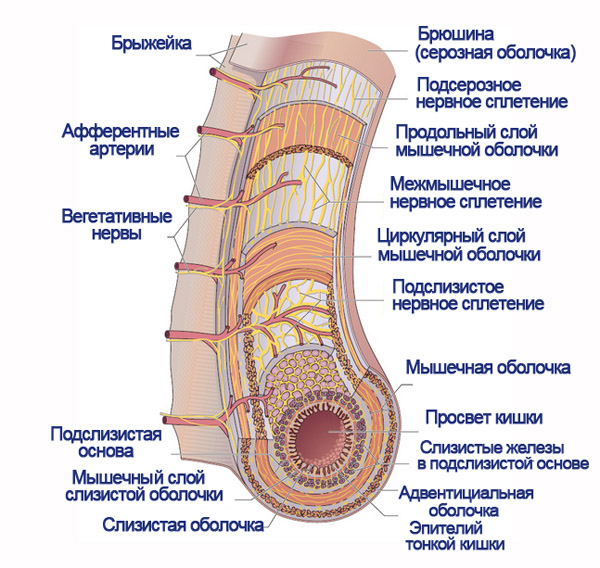
Расщепление в кишечнике
Не все белки подвергаются полному распаду в кишечнике, хотя над этим трудится много веществ. Даже в конце переваривания могут оставаться дипептиды и трипептиды. Лишь некоторые аминокислоты выходят из этого отдела ЖКТ единичными.
Трипсин и хемотрипсин помогают белкам преобразоваться в полипептиды, выделяя при нехватке глюкозы в организме тепло, здесь продолжает свое действие энергетическая функция белков. Примеры такого преобразования мы можем наблюдать каждый день, когда употребляем различные вещества в пищу. После распада белков на полипептиды вступает в работу фермент карбоксиполипептаза — она отсоединяет отдельные аминокислоты от конца образовавшихся соединений. Проэластаза переваривает эластические волокна мясных продуктов и других сложных веществ.
Белки, выполняющие энергетическую функцию, проходят последний этап своего расщепления в тонком кишечнике, двенадцатиперстной кишке. Там они подвергаются воздействию ворсинок, которые содержат в себе пептидазы. Эти вещества, взаимодействуя с кишечной жидкостью, заканчивают процесс расщепления полипептидов до маленького числа аминокислот. Далее процесс распределения тепла как энергии от распада белков происходит на клеточном уровне, а конечными продуктами расщепления этих сложных по структуре веществ являются мочевая кислота, мочевина, вода и углекислый газ. Таким образом, мы увидели, где осуществляется энергетическая функция белков. Она не имеет конкретного места локализации аминокислот. Но осуществляется она от начала и до полного расщепления белка.