Степени дисплазии шейки матки
Содержание:
- Диагностика:
- Лечение дисплазии шейки матки
- Причины
- Дифференциальная диагностика
- Диагностика дисплазии шейки матки
- Профилактика
- Патология плоского эпителия lsil
- Цены на различные методы лечения
- Чем опасна дисплазия во время беременности
- Методики лечения дисплазии CIN 2
- Как лечить дисплазию шейки матки
- Как и почему возникает неоплазия
- Почему лечение дисплазии шейки матки 1 степени классическими методами зачастую заканчивается рецидивом
- Ампутация шейки матки — в каких случаях и как часто применяется?
Диагностика:
- осмотр шейки матки в зеркалах;
- визуальная оценка шейки матки после обработки уксусной кислотой (VIA);
- цитологическое исследование;
- ВПЧ-тестирование;
- кольпоскопия;
- биопсия шейки матки.
Верификация при патологоанатомическом исследовании биопсийного материала.
2.1 Жалобы и анамнез
Анализ анамнеза.
Факторы риска CIN:
- раннее начало половой жизни;
- большое число и частая смена половых партнеров;
- курение;
- половые инфекции;
- большое число беременностей и родов;
- иммунокомпрометирующие заболеваний (гепатиты B, С, ВИЧ);
- иммуносупрессивная терапия;
- длительный прием КОК.
«Контактные» кровянистые выделения из половых путей:
- длительность,
- анамнез хирургических вмешательств на шейке матки,
- ВПЧ-инфекции,
- результаты ранее проведенного цервикального скрининга.
CIN I/II/III и CIS диагностируются только морфологическими методами.
2.2 Физикальное обследование
Осмотр влагалища и шейки матки в зеркалах:
- CIN визуально не определяется;
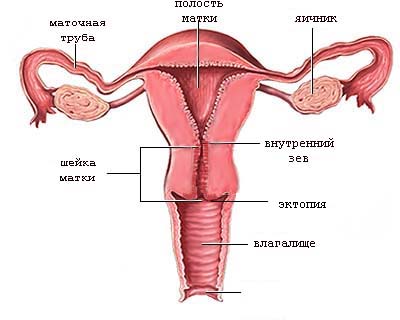
- эктропион — цилиндрический эпителий на экзоцервиксе, иногда в сочетании с деформацией наружного зева;
- истинная эрозия — на неизмененном экзоцервиксе ярко-красный дефект с четкими неправильными краями, нередко с отеком, расширением сосудов, фибринозным налетом и контактной кровоточивостью.
2.3 Лабораторные диагностические исследования
Для выявления CIN цитологическое исследование микропрепарата шейки матки:
- всем женщинам 21-65 лет с интервалом в 3 года;
- моложе 21 года при половой жизни более 3 лет;
- для выявления CIN II чувствительность – 68,9%, специфичность – 97,2%;
- низкая воспроизводимость повторных мазков в течение 1,5 мес. после первичных;
- пересмотр аномальных мазков;
- 10% мазков неинформативны из-за неправильной техники забора и подготовки препарата;
- наиболее эффективная жидкостная цитология.
Молекулярно-биологическое исследование отделяемого из цервикального канала на все ВПЧ (не менее 12 типов):
- женщинам 30-65 лет;
- старше 30 лет скрининг каждые 5 лет;
- старше 30 лет у ВПЧ-позитивных женщин ежегодный скрининг;
- в любом возрасте при цитологии ASCUS, ASC-H, LSIL, HSIL.
2.4 Инструментальные диагностические исследования
Расширенная кольпоскопия:
- при визуальных изменениях шейки;
- при аномалиях в мазках от ASCUS и более;
- при положительном тесте на ВПЧ ВКР;
- для выбора места и метода биопсии шейки матки для верификации диагноза;
- при невозможности — VIA (осмотр шейки после 3% уксусной кислоты).
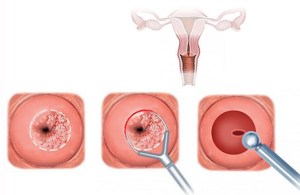
Прицельная биопсия шейки матки (punch-биопсия) при кольпоскопии:
- при необходимости мультифокальная биопсия;
- при ASCUS, ASC-H, LSIL с ВПЧ ВКР;
- при аномальной кольпоскопической картине.
При HSIL:
- прицельная биопсия или эксцизия зоны трансформации (ЗТ) шейки с последующим выскабливанием цервикального канала и гистологией;
- женщинам старше 50 лет и/или с зоной трансформации III типа целесообразна конизация шейки.
Для диффдиагностики степени тяжести поражения шейки — определение индекса пролиферативной активности экспрессии:
- p16/Ki67 при ИЦХ или
- р16 в при ИГХ.
Лечение дисплазии шейки матки
При легкой степени предракового перерождения клеток назначается консервативное лечение – противовоспалительные препараты, противовирусные средства, общеукрепляющая терапия. Его длительность не должна превышать 3 недель. В случае неэффективности патологические очаги удаляют.
Хирургическое лечение проводят с помощью лазера, радионожа, фотодинамической (световой) терапии. Методы позволяют убрать патологические очаги на слизистой без образования рубцов. Эластичность тканей полностью сохраняется, что дает возможность лечить женщин, которые впоследствии планируют беременность и роды.
Лазер в медицине

Радиоволновой аппарат
При выраженной дисплазии, особенно при подозрении на начавшееся раковое перерождение, назначается конизация – удаление конусообразного участка тканей шейки и цервикального канала с помощью лазера, радионожа или хирургического инструмента. Полученные образцы передают на гистологическое исследование с целью выявления злокачественных клеток.
Профилактикой болезни служит своевременное выявление папилломавируса с последующим проведением противовирусных мероприятий, а также борьба с факторами, провоцирующими заболевание.
При подозрении на наличие заболевания нужно обратиться в Университетскую клинику для диагностики и лечения этого опасного состояния.
Причины
Чтобы онкологический процесс начал развиваться на фоне инфицирования организма вирусом папилломы человека, необходимо воздействие на него ряда определенных факторов
Также нужно принимать во внимание, что ВПЧ не всегда является причиной появления неоплазии первой степени
С того момента как произойдет заражение, или он активизируется и запустит процесс развития предракового состояния, может пройти от полутора до пяти лет. Сам рак может формироваться в течение длительного периода времени (несколько лет или десятилетий).
Если говорить о неоплазии, то такому состоянию могут способствовать сразу несколько причин:
- определенный вид ВПЧ;
- ранняя половая жизнь;
- множество половых партнеров;
- прием препаратов, в составе которых присутствуют гормоны, на протяжении длительного времени;
- курение и чрезмерное употребление алкогольной продукции;
- ослабленная иммунная система;
- многочисленные аборты или другие виды оперативного вмешательства;
- сбой гормонального фона;
- генетическая предрасположенность;
- патологии инфекционной природы происхождения, затрагивающие женскую половую систему.
Но в большинстве случаев основным провоцирующим фактором становится именно папилломавирус. При этом патология может первое время развиваться без проявления клинической картины.
Дифференциальная диагностика
Белыми пятнами и бляшками, которые нужно дифференцировать с лейкоплакией, проявляются химические поражения слизистой, сифилитические папулы, кандидозные поражения, псориаз, рубцующийся эритематоз, белый губчатый невус, красный плоский лишай.
Кроме того, даже отдифференцировав другие белые пятна или бляшки, еще не решен вопрос, что же представляет собой лейкоплакия в конкретном случае, поскольку клинически невозможно определить гистологические изменения, патогномоничные для лейкоплакии. По существу, поставив клинический диагноз лейкоплакия, мы не можем предложить метод лечения, так как не знаем точно, с чем имеем дело: или с «мозолью» на слизистой, или с предраковым состоянием, или с инвазивным раком. И все эти состояния попадают под клинический диагноз лейкоплакия.
Диагностика дисплазии шейки матки
Для ранней диагностики предраковых поражений шейки матки во многих странах мира существует система цервикального скрининга.
В России данная система включает последовательность действий:
- Цитологическое исследование: РАР-тест;
- ВПЧ-тестирование: в США и странах Евросоюза ВПЧ-тест применяется для первичного скрининга рака шейки матки (РШМ). В России его использование вариативно: при первичном скрининге в сочетании с РАР-тестом, в качестве самостоятельного теста, при ведении пациенток с неясными результатами РАР-теста (ASCUS) и для наблюдения паценток после лечения HSIL;
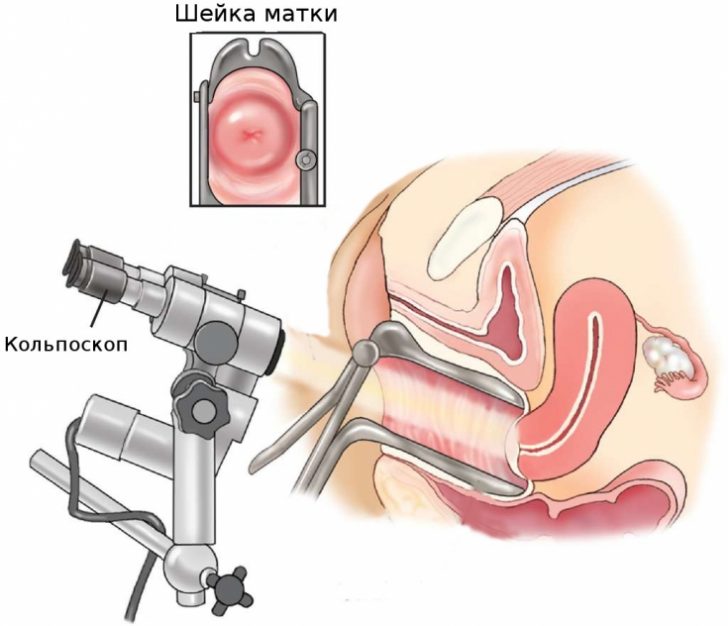
- Кольпоскопия: показаниями к исследованию являются положительные результаты РАР-теста (класс 2-5). Метод основан на осмотре шейки матки при помощи увеличивающих оптических систем и проведения диагностических проб с растворами уксусной кислоты и йода (Люголя). С помощью кольпоскопии определяют локализацию поражения, его размер, выбирают участок для проведения биопсии, определяют тактику лечения.
При кольпоскопии должна быть тщательно оценена зона трансформации (переходная зона стыка двух видов покровного эпителия шейки матки).
Влагалищная часть шейки матки (экзоцервикс) покрыта многослойным плоским эпителием. В канале шейки матки (цервикальном канале, эндоцервиксе) — цилиндрический эпителий. Место перехода цилиндрического эпителия цервикального канала в многослойный плоский эпителий поверхности шейки матки носит название зоны трансформации. Эта область имеет большое клиническое значение, поскольку именно в ней возникает более 80% случаев дисплазии и рака шейки матки.
- Зона трансформации 1 типа — переходная зона видна полностью. Это самый оптимальный и прогностически «благоприятный» вариант кольпоскопического заключения.
- Зона трансформации 2 типа — переходная зона частично скрыта в канале шейки матки. Адекватно оценить такую картину сложно, так как наиболее измененные участки могут быть не видны и пропущены.
- Зона трансформации 3 типа — переходная зона находится глубоко в канале шейки матки и оценить её кольпоскопически невозможно. Кольпоскопия в этом случае считается неинформативной, поскольку глубина залегания патологического очага остается неизвестной.
Биопсия: прицельная или расширенная биопсия (конизация) всегда должна выполняться под контролем кольпоскопии. Выбор метода биопсии зависит от типа поражения, возраста пациентки и зоны трансформации
Важной информацией, которую дает биопсия, является возможность иммуногистохимического определения маркера ранней диагностики дисплазии с высокой степенью риска озлокачествления: p16INK4a
Профилактика
Профилактика РШМ (ВОЗ, 2014):
- первичная -вакцинация против ВПЧ девочек 9-13 лет и до начала половой жизни;
- вторичная – скрининг и лечение предрака шейки матки.
Стратегии скрининга
21-29 лет:
- цитология/жидкостная цитология 1 раз в 3 года;
- ниже ASCUS – повторить цитологию (ПАП-тест) через 3 года;
- при аномалиях выше ASCUS — ВПЧ-тест;
- при ASCUS и ВПЧ-тест (-) – повторно ко-тестирование через 3 года;
- при ASCUS и ВПЧ-тест (+) – кольпоскопия с биопсией шейки матки.
30-65 лет предпочтительный вариант:
- ко-тестирование (цитология/жидкостная и ВПЧ тест);
- цитология (ПАП-тест) при:
- < ASCUS и ВПЧ (-) – повторное ко-тестирование через 5 лет,
- = ASCUS и ВПЧ (-) – повторное ко-тестирование через 3 года,
- < ASCUS и ВПЧ (+) – повторное ко-тестирование через 1 год,
- ≥ ASCUS и ВПЧ (+) — кольпоскопия и биопсия шейки,
- < ASCUS или = ASCUS и ВПЧ (+) – кольпоскопия и биопсия шейки;
- HSIL и ВПЧ (+/-):
- старше 25 лет – кольпоскопия и петлевая эксцизия или конизация,
- младше 25 лет – кольпоскопия и биопсия шейки матки.
30-65 лет допустимый вариант — на первом этапе ВПЧ-тестирование:
- ВПЧ (-) – повторный ВПЧ-тест через 5 лет;
- ВПЧ (+) — ПАП-тест.
Профосмотры или диспансеризация:
- I группа здоровья:
- 21-29 лет – цитология 1 раз в 3 года,
- 30-65 лет – цитология и ВПЧ-тест 1 раз в 5 лет;
- II группа здоровья — при наличии факторов риска, ВПЧ (+) — цитология (ПАП-тест:
- ≥ ASCUS – кольпоскопия,
- < ASCUS – повторное ко-тестирование через 1 год;
- III группа здоровья– лечение доброкачественных заболеваний шейки матки.
После хирургического лечения HSIL:
- ко-тестирование (цитология и ВПЧ – тест):
- первый через 3 месяца,
- затем каждые 6 месяцев 2 года,
- далее ежегодно 20 лет;
- рецидив:
- расширенная кольпоскопия и реконизация;
- консультация врача-онколога (по показаниям);
- иногда гистерэктомия при рецидиве CIN II/III.
Диспансерное наблюдение
Цитология:
- при LSIL 1 раз в 6 месяцев в течение 18-24 месяцев;
- после хирургического лечения LSIL с ВПЧ-тестом через 6-12 месяцев;
- после хирургического лечения HSIL с ВПЧ-тестом по схеме 29 лет (смотри выше).
Организация оказания медицинской помощи
Эксцизионное и аблативное лечение предпочтительно амбулаторно или в дневном стационаре.
Показания для госпитализации:
- ножевая конизация шейки матки с диагностическим выскабливанием цервикального канала и полости матки;
- эксцизия шейки матки (при невозможности амбулаторной).
Патология плоского эпителия lsil
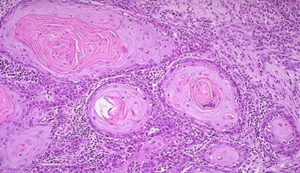
Дисплазия шейки матки — это патологические изменения в клетках на поверхности шейки матки или аномальный рост предраковых клеток на поверхности шейки матки, которые видны под микроскопом. Альтернативные названия: цервикальная интраэпителиальная неоплазия (CIN), предраковые изменения шейки матки.
Сами по себе эти изменения не являются раком. Это состояние классифицируется как низкая степень или высокая злокачественности, в зависимости от степени роста аномальных клеток.
Низкая степень дисплазии шейки матки прогрессирует очень медленно и часто нормализуется сама по себе. Тем не менее, она может привести к раку шейки матки без надлежащего лечения.
Без лечения 30 — 50% случаев тяжелой дисплазии шейки прогрессирует в инвазивный рак. Риск заболевания раком ниже, в случае умеренного роста.
Дисплазия шейки матки напрямую связана с вирусом папилломы человека (ВПЧ), передающимся половым путем вирус.
Признаки и симптомы дисплазии шейки матки
Дисплазия шейки матки часто не имеет симптомов, и, как правило, обнаруживается в ходе исследования мазка на онкоцитологию (мазок Папаниколау).
Иногда признаки и симптомы могут включать:
— Остроконечные кондиломы — Аномальное менструальное кровотечение — Незначительные кровянистые выделения после полового акта — Влагалищные выделения между менструациями
— Боль в пояснице
Эти симптомы так же могут быть вызваны другими заболеваниями, поэтому очень важно обратиться к врачу для постановки точного диагноза
Причины дисплазии шейки матки
Точная причина дисплазии шейки матки не известна. Исследования показали сильную связь между дисплазией шейки матки и инфекцией вируса папилломы человека (ВПЧ).
ВПЧ является распространенным вирусом, который передается через половой контакт. Есть много различных типов ВПЧ. Некоторые типы привести к развитию дисплазии шейки матки или раку.
Дисплазия шейки матки чаще наблюдается у женщин в возрасте от 25 — 35 лет, но может развиться в любом возрасте.
Следующие факторы могут увеличить риск развития дисплазии шейки матки:
— Начало ранней половой жизни; — Раннее рождение ребенка (до 16 лет); — Наличие нескольких сексуальных партнеров; — Наличие партнера, чей бывший партнер имел рак шейки матки — Прием препаратов, которые подавляют иммунную систему — Курение — Вирус папилломы человека (ВПЧ) — Остроконечные кондиломы — История одного или нескольких венерических заболеваний, таких как генитальный герпес или ВИЧ — Химиотерапия — Использование противозачаточных пилюль в течение более 5 лет — У женщин, чья мать применяла диэтилстильбестрол (DES), чтобы забеременеть или для поддержания беременности. Этот препарат использовался в 60-е годы, чтобы предотвратить выкидыш. — Низкий уровень фолиевой кислоты (витамин В9) в красных кровяных клетках
— Недостаток витамина А, бета-каротина, селена, витамина Е и витамина С.
Диагностика дисплазии шейки матки
Для диагностики и скрининга дисплазии шейки матки ежегодно проводится Пап-тест (мазок на онкоцитологию, мазок Папаниколау) даже при отсутствии симптомов.
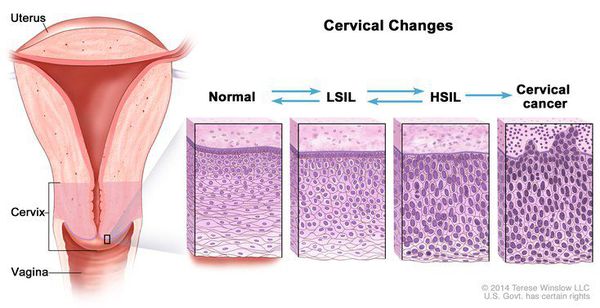
Дисплазия шейки матки, что видна в результатах мазка Папаниколау называют плоскоклеточным интраэпителиальным поражением (SIL). Эти изменения могут быть:
— Низкая степень плоскоклеточного интраэпителиального поражения (LSIL) — Высокая степень плоскоклеточного интраэпителиального поражения (HSIL) — Начальная степень рака (злокачественное поражение)
— Атипичные железистые клетки (AGUS)
Гинекологический осмотр, как правило, малоэффективен в диагностики дисплазии, поэтому если есть какие-либо сомнительные или неясные результаты мазка Папаниколау, то требуются иные диагностические мероприятия для изучения степени поражения и злокачественности:
— Кольпоскопия — Цервикальная биопсия — Тест ДНК ВПЧ
— Конусная биопсия (конизация)
Степени дисплазии шейки матки
Результаты Пап-мазка основаны на основе медицинской системы терминологии, называемой системой Бетесда (Bethesda), которая была разработана в Национальном институте здоровья США штата Мэриленд в 1988 году и изменена в 2001 году. Основные категории для оценки ненормальных результатов мазка Папаниколау заключаются в следующем:
Atypical squamous cells
Атипичные клетки плоскоклеточного эпителия неясного значения
Слово “плоскоклеточный” описывает тонкие, плоские клетки, которые лежат на поверхности шейки матки. Один из двух вариантов добавляется в конце ASC:
- ASC-US, что означает атипичные клетки плоского эпителия неясного значения
- ASC-H, атипичные клетки плоского эпителия, не позволяющие исключить HSIL
Low grade squamous intraepitelial lesion
Цены на различные методы лечения
Лечение дисплазии может проводиться консервативным или оперативным способом.
При консервативном методе в стоимость лечения включают: осмотр, анализы, диагностические мероприятия (кольпоскопию, биопсию). Консультации (в зависимости от уровня клиники) стоят от 500 рублей до 3 – 5 тысяч, диагностика – до 1 тысячи рублей за каждый анализ или процедуру.
Оперативное вмешательство может проводиться разными способами, поэтому цена зависит от выбранной методики:
- кононизация – от 1 тыс. руб.;
- лазер – от 1,5 тыс. руб.;
- радиоволновой метод – от 500 рублей;
- прижигание – не более 700, в среднем 200 – 500 рублей;
- криодеструкция – от 1,5 тыс. руб.;
- удаление матки – от 5 тыс. руб.
Чем опасна дисплазия во время беременности
Последнюю стадию дисплазии у беременных диагностируют редко, поскольку в период ожидания малыша женщина регулярно посещает гинеколога. Для подтверждения диагноза необходимо сдать повторно анализы.
Биопсия – один из наиболее результативных методов диагностики, но для беременных оно опасно – увеличивается риск выкидыша. Но дисплазия несет опасность не только здоровью, но и жизни женщины, поэтому по медицинским показаниям делать биопсию необходимо.
Чаще всего медикаментозное и лечение и операцию врачи проводят после родов. Но всю беременность будущей маме придется находиться под постоянным наблюдением врача в стационаре.
Методики лечения дисплазии CIN 2
Медикаментозный метод в чистом виде, без удаления патологических очагов, применяется крайне редко в случае неглубоких поражений, при отсутствии прогрессирования и при противопоказаниях к хирургическому лечению. Он подразумевает прием антивирусных и общеукрепляющих препаратов. Лечение проводится не более 6 месяцев, под строгим наблюдением за результатами.
Метод применяется при степени поражения CIN 1, но иногда оказывается успешным и при CIN 2. В случае активизации иммунной системы, позволяющей побороть вирус, проявления интраэпителиальной неоплазии исчезают без дополнительных местных процедур. Но все-равно, впоследствии пациентка должна периодически посещать гинеколога для выявления возможного рецидивирования болезни.
При неэффективности консервативных методов диспластические очаги удаляют с помощью аппаратных методов:
- Электрокоагуляцией — прижиганием током. Методика применяется достаточно редко, поскольку высокая температура обжигает и губит здоровые клетки. Это приводит к образованию рубцовой деформации шейки матки и проходящего внутри нее цервикального канала. Впоследствии у женщины могут быть проблемы с раскрытием шеечного канала при родах.
- Криодеструкцией — замораживанием патологических очагов жидким азотом. При таком методе сложно спрогнозировать глубину проникновения хладагента. В результате могут погибнуть здоровые клетки или, наоборот, остаться измененные. Поэтому эта методика тоже применяется ограниченно.
- Лазерным методом — современным способом лечения, при котором на пораженную область воздействуют лазерным лучом. Методика вызывает закипание жидкости внутри патологических клеток и их гибель. На месте воздействия формируется корочка, которая потом отпадает с образованием гладкого ровного эпителия. При этом не образуются жесткие рубцы и участки деформации, а эластичность тканевых структур остается в норме. Поэтому лазер может применяться у женщин, планирующих в перспективе еще рожать детей.
- Радиоволновым методом (радионожом), при котором на патологический очаг воздействуют высокочастотными радиоволнами, нагревающими жидкость внутри клеток. В результате диспластический участок испаряется. После тканевого заживления также не остается грубых рубцов и других выраженных изменений. Радионож подходит для женщин детородного периода.
Как лечить дисплазию шейки матки
При определении тактики ведения больной с данной патологией учитывают выраженность обнаруженных изменений, возраст пациентки, репродуктивную функцию и дальнейшие планы на деторождение. Современные методы диагностики диспластических изменений шейки матки, оптимизация лечения является надежным методом профилактики серьёзных осложнений.
1. Операция при дисплазии шейки матки
При легкой степени дисплазии (1 ст.) это — радиоволновое лечение путем создания термического повреждения на глубину 5-7 мм для уничтожения потенциально диспластического эпителия, лежащего под зоной трансформации. Специалисты, в том числе и врачи нашей клиники, не рекомендуют использование метода криодеструкции или лазерной вапоризации для лечения дисплазии шейки матки 2 и 3 степени ввиду не всегда предсказуемой глубины некроза и невозможности послеоперационного гистологического контроля. Пациенткам старше 40 лет показаны методы эксцизии или конизация дисплазии шейки матки тяжелой степени или при раке in situ, с обязательным исследованием ступенчатых срезов удалённой части органа.
При тяжелой дисплазии и внутриэпителиальной онкологии (рак in situ), показана консультация онкогинеколога с последующим выполнением конизации экзоцервикса с выскабливанием оставшейся части цервикального канала и, по показаниям, полости матки. У пациенток в постменопаузе с раком in situ, расположенным в переходной зоне в цервикальном канале, методом выбора является экстирпация матки.
2. Петлевая электроконизация
Петлевая электроконизация шейки матки или LEEP (Loop Electrosurgical Excision Procedure) или LLEETZ (Large Loop Electrosurgical Excision of Transformation Zone). Это хирургическое вмешательство, состоящее в иссечении тонкого слоя аномальной ткани при помощи электрического тока и радиоволны, поступающего через тонкие петли — электроды. Полученный образец ткани направляется на гистологию. В нашей клинике процедура конизации при дисплазии шейки матки проводится современным радиоволновым методом.
3. Конизация шейки матки при дисплазии
Эта лечебная процедура включает удаление конического участка ткани шейки матки с явлениями дисплазии. Основание конуса образуют ткани экзоцервикса (влагалищной части шейки матки), а вершину — ткани цервикального канала. Зона трансформации (граница между экзо- и эндоцервиксом) включена в конический образец тканей. При гистологическом подтверждении диагноза и отсутствии опухолевых клеток в краях резекции и соскобе из цервикального канала проведенный объем хирургического вмешательства считается адекватным.
4. Медикаментозное лечение
Вспомогательный метод, применяется при лечении шейки или цервикального канала с начальной (легкой) степенью дисплазии, либо в качестве дополнения к оперативному.
ПОСЛЕОПЕРАЦИОННЫЙ ПЕРИОД
После деструктивных методов лечения дисплазии осмотр шейки матки и кольпоскопию проводят через 6-8 недель. При дисплазии 1 степени показано наблюдение (осмотры, включающие кольпоскопию и цитологическое исследование) каждые 6 мес в течение 2 лет. Наблюдение (осмотры, включающие кольпоскопию и цитологическое исследование) за пациентками, лечившимися по поводу ЦИН 1, 2 показано 1 раз в 3 мес. в течение первого года и 2 раза в год в последующем. При хороших результатах кольпоскопии и жидкостной онкоцитологии, отсутствии онкотипов ВПЧ пациентку можно перевести на обычный режим скрининга шейки матки.
Наличие признаков дисплазии в краях эпителия удаленного образца шейки матки свидетельствует о высоком риске рецидива, но не является поводом для повторной эксцизии, если:
- зона трансформации полностью визуализируется;
- нет признаков железистой патологии;
- нет признаков инвазии;
- возраст женщины менее 50 лет.
Женщины старше 50 лет с неполным удалением дисплазии и позитивными эндоцервикальными краями — группа риска по остаточному (резидуальному) заболеванию шейки матки. Адекватное наблюдение — минимальное требование в данной ситуации. Альтернативным методом лечения дисплазии шейки матки при остаточных явлениях процесса является повторная конизация. Удаление матки показано пациенткам со стойкими тяжёлыми поражениями, отягощенными наличием осложненного гинекологического анамнеза.
home
Лечение дисплазии шейки матки в Москве
Есть необходимость попасть к хорошему специалисту по дисплазии шейки матки? Клиника на Кутузовском и ее гинекологи предлагают полный спектр услуг от диагностики и удаления патологии до ежегодной профилактики. Не откладывайте на завтра заботу о собственном здоровье!
Цены
на услуги Запись
к врачам
Как и почему возникает неоплазия
Причина цервикальной неоплазии (CIN) – инфицирование папилломавирусом. Наиболее часто его вызывают штаммы (типы) 16, 18 и 31, однако заболевание может быть спровоцировано и другими разновидностями возбудителя.
Вирус папилломы человека передается в основном половым путём. После попадания в организм он долгое время может никак себя не проявлять. Более чем у половины женщин инфекция не развивается, поскольку возбудителя убивает иммунная система. В остальных случаях спустя какое-то время вирус, попадая на слизистую шейки, нарушает процесс клеточного деления.
В тканях образуются неправильно развитые, уродливые, слишком большие или маленькие, двухъядерные, деформированные клетки. Эти клеточные структуры называют диспластическими или неопластическими, а вызванные ими заболевания – цервикальной интраэпителиальной неоплазией (CIN) шейки. Процесс вначале захватывает только верхний слой слизистой, а затем начинает проникать всё глубже. В итоге образуется карцинома in situ – рак на месте, не прорастающий глубоко и не дающий метастазов, который позже переходит в инвазивную опухоль с прорастанием в соседние ткани и метастазированием.
В 80% случаев развивается плоскоклеточный рак, поражающий эпителий эктоцервикса – наружной части шейки, в 10% случаев – аденокарцинома или железистый рак, который формируется внутри цервикального канала, идущего от матки к влагалищу. Иногда развиваются более редкие виды злокачественных опухолей – светлоклеточные, мукоэпидермоидные, карциноид. Может возникнуть смешанная форма онкологии, состоящая из нескольких видов клеток.
Развитие заболевания провоцируют:
- Заражение различными вирусными и бактериальными инфекциями. У женщин, заражённых кроме папилломавируса вирусом герпеса, цитомегаловирусом, хламидиями и микоплазмами, риск дисплазии увеличен в 3-4 раза.
- Воспалительные процессы – цервицит (воспаление шейки), эндоцервицит (воспаление цервикального канала), эктоцервицит (воспаление слизистой, покрывающей шейку), кольпит (воспаление слизистой половых путей). Эти заболевания снижают местный тканевый иммунитет и способствуют развитию болезни.
- Слишком раннее начало интимной жизни. По данным научных исследований, начало сексуальной жизни раньше 14 лет 20-кратно увеличивает риск заражения ВПЧ и возникновения неоплазии.
- Беспорядочная половая жизнь без применения барьерных методов защиты.
- Аборты и тяжёлые роды, сопровождавшиеся травматизацией тканей.
- Гормональный дисбаланс.
- Дисбиоз влагалища – состояние, при котором в половых путях погибают полезные микроорганизмы и усиленно размножаются патогенные.
- Курение – доказано, что раковые и предраковые патологии у курящих женщин возникают гораздо чаще.
- Неблагоприятная наследственность.
- Сниженный иммунитет, при котором организм не может бороться с вирусом. Сочетание ВИЧ-инфекции и цервикальной неоплазии встречается достаточно часто. На фоне снижения иммунитета поражение быстро прогрессирует, поэтому всем женщинам, у которых обнаружена неоплазия, рекомендуется сдать кровь на ВИЧ.
Почему лечение дисплазии шейки матки 1 степени классическими методами зачастую заканчивается рецидивом
Согласно рекомендациям Минздрава, лечение CIN 1 не проводится. Если биопсия подтверждает дисплазию слабой степени, женщину отпускают под наблюдение – считается, что в 90% случаев выздоровление наступает самопроизвольно и лечение ЦИН 1 не требуется.
Сама биопсия (кусочек ткани шейки матки) в случае CIN I уже может оказаться не только диагностической, но и лечебной процедурой, когда пораженный участок удаляется вместе с забранным материалом.
При отсутствии кольпоскопических признаков ВПЧ инфекции и нормальной вирусной нагрузке я также склоняюсь к наблюдению LSIL.
В некоторых случаях на фоне легкой дисплазии назначается лазерная абляция (прижигание) эпителия или радиоволновая эксцизия – удаление участка пораженной ткани.
Но иногда, вопреки всем рекомендациям, при LSIL выполняется конизация и даже удаление всех гениталий (когда дисплазия сочетается, например, с миомой матки). Я расцениваю такой подход как неоправданный лечебный риск – это когда риск проводимого лечения превышает риск самого заболевания.
Дело в том, что и биопсия, и эксцизия, и конизация, и удаление гениталий позволяют устранить диспластический эпителий. Но причина вирусной дисплазии – ВПЧ – остаётся. А так как любое лечебное воздействие само по себе является для вируса провоцирующим фактором, это приводит к высокому проценту рецидивов.
Противовирусные препараты сегодня не показывают эффекта в подавлении вируса, поэтому целесообразность их назначение остается под большим сомнением.
Минздрав рекомендуют начинать лечение только в том случае, если дисплазия LSIL переходит в стадию HSIL.
С такой тактикой я тоже не могу согласиться.
Запомните!
если в цитологическом анализе обнаружены атипические клетки,
если CIN I по данным кольпоскопии сопутствуют очевидные вирусные признаки папилломавирусной инфекции,
если иммуногистохимическое исследование показывает экспрессию белка р16,
ТО ПРИМЕНЕНИЕ НАБЛЮДАТЕЛЬНОЙ ТАКТИКИ ВАМ ПРОТИВОПОКАЗАНО!
Эти факторы говорят об активном процессе и требуют незамедлительного лечения.
Международное медицинское сообщество особенно акцентирует внимание на том, что любой случай инвазивного рака шейки матки – всегда есть упущенная возможность своевременной диагностики и лечения дисплазии
И свою первоочередную задачу я вижу в том, чтобы не дать всем думающим женщинам пополнить статистику упущенных возможностей.
Ампутация шейки матки — в каких случаях и как часто применяется?
В сравнении с конизацией, ампутация (от лат. amputare – усекать, отсекать, удалять) шейки матки – более травматичная и объёмная операция.
В случаях цервикальной дисплазии ампутацию применяют тогда, когда полноценную конизацию сделать невозможно. Например, из-за значительной деформации шейки матки или сочетанной с дисплазией шеечной патологии.
Операция проводится в стационаре, как правило, под общим наркозом.
Режущим инструментом обычно бывает хирургический скальпель. Но могут применяться электохирургические или ультразвуковые методики.
- Клиновидная ампутация по Шредеру
- Ампутация по Штурмдорфу
Клиновидная ампутация шейки матки
- Изолированная элонгация шейки матки
- Атрофическая деформация ШМ в пожилом возрасте
- Травматическая деформация (разрывы после родов, послеоперационные травмы, эктропион, др.)
- Гиперплазия поражённых шеечных желёз в подслизистом слое ШМ
Суть оперативной техники
Намеченную к удалению часть шейки матки рассекают на две половины. Из полученных одной или обеих частей шейки вырезают клиновидный участок, включающий зону поражения в пределах здоровой ткани.
Оставшиеся лоскуты сшивают между собой отдельными швами так, что в результате слизистая цервикального канала смыкается с образованием нового наружного зева (отверстия).
Клиновидная ампутация шейки матки
Технику такой ампутации впервые предложил немецкий врач акушер-гинеколог Карл Шредер ещё в ХІХ веке. С тех пор операция носит его имя.
Конусовидная ампутация шейки матки
- Те же, что при клиновидной ампутации
- Обширное аномальное поражение влагалищной части ШМ
- Обширное аномальное поражение цервикальной слизистой внутри канала
- Неясная картина поражения с подозрением на инвазивный злокачественный процесс
В сравнении с клиновидной, конусовидная ампутация носит более радикальный характер.
- Низкую конусовидную ампутацию ШМ – в этом случае удаляется «макушка» наружной части шейки матки
- Среднюю
- Высокую – предполагает ампутацию конусовидного фрагмента шейки матки по всей длине цервикального канала, вплоть до внутреннего зева тела матки
Высокую ножевую конусовидную ампутацию рассматривают хорошим вариантом органосохраняющего лечения преинвазивного (ТisN0M0) и микроинвазивного (Т1аN0M0) рака шейки матки у женщин детородного возраста.
Суть оперативной техники
Отступив 5-10 мм от границы области поражений, делают круговой разрез слизистой шейки. При этом слизистую несколько отделяют скальпелем от мышечной ткани.
Затем разрез на шейке углубляют в толщу по направлению цервикального канала. Вырезают и вынимают конусообразный сегмент.
В завершение «натягивают» отсепарированную ранее слизистую на раневую поверхность, оставляя свободным просвет цервикального канала и формируя «новую» шейку. Рану на шейке ушивают отдельными или модифицированными швами.
Конусовидная ампутация шейки матки по А. Штурмдорфу
Технику конусовидной ампутации ШМ разработал американский гинеколог А. Штурмдорф в начале ХХ века. Изначально её проводили для лечения гипертрофии и хронического воспаления влагалищной части шейки матки.
В настоящее время обе вышеописанные операции в лечении тяжёлой дисплазии имеют второстепенное значение и применяются ограничено.
Высокая ампутация
Высокая ампутация шейки матки – полное удаление шейки до границ внутреннего зева матки с иссечением верхнего отдела влагалища.
Объём оперативного вмешательства при высокой ампутации шейки матки
- Совмещённая патология шейки на фоне здорового тела матки
- Распространение дисплазии на своды влагалища
Высокая ампутация ШМ – серьёзная лечебно-реконструктивно-пластическая операция.
Проводится: — в клиническом стационаре;
— под общим или эпидуральным наркозом;
— влагалищным или комбинированным с лапароскопией доступом.
Несмотря на максимальный объём удаления шейки, эта органосохраняющая хирургическая методика оставляет женщине возможность вести полноценную интимную жизнь, зачать, выносить и родить ребёнка.