Анализ крови на антитела
Содержание:
- Лечение иммунологического бесплодия
- Функции антител [ править | править код ]
- Какие органы участвуют в образовании антител
- 3.1 Антитела
- Что означает снижение числа антител для образования коллективного иммунитета?
- История изучения
- История изучения
- Антитела при беременности
- Ответы на частые вопросы
- Какими бывают защитные барьеры организма
- Лекция 3 Генетическая основа разнообразия специфичности активных центров антител
- Какие бывают антитела к щитовидке и почему они появляются
- Антитела к бактерии Helicobacter pylori
- Память иммунной системы
- Диагностика туберкулеза
- Вариабельность антител
Лечение иммунологического бесплодия
- Для снижения выработки АСАТ женщине вводят аллогенные лимфоциты партнёра, подавляющие излишнюю активность иммунной системы. Этот метод «приучает» иммунитет к чужеродным белковым соединениям. Применяются препараты, разжижающие слизистую шейки матки и облегчающие проникновение сперматозоидов внутрь.
- Мужчине назначают противовоспалительные средства и препараты, снижающие повышенную активность иммунной системы.
- Проводится лечение инфекций, в том числе ЗППП.
- После курса лечения возможно наступление беременности естественным путем, с помощью внутриматочного введения семенной жидкости, методов ЭКО и ИКСИ.
Функции антител [ править | править код ]
Иммуноглобулины всех изотипов бифункциональны. Это означает, что иммуноглобулин любого типа распознает и связывает антиген, зачастую нейтрализуя его вред для организма, а затем активирует эффекторные механизмы иммунитета на борьбу с источником этих антигенов.
Одна область молекулы антител (Fab) определяет её антигенную специфичность, а другая (Fc) осуществляет эффекторные функции: связывание с рецепторами, которые экспрессированы на клетках организма (например, фагоцитах); связывание с первым компонентом (C1q) системы комплемента для инициации классического пути каскада комплемента.
- IgG (молекулярная масса 146 кДа) является основным иммуноглобулином сыворотки здорового человека (составляет 70-75 % всей фракции иммуноглобулинов), наиболее активен во вторичном иммунном ответе и антитоксическом иммунитете. Благодаря малым размерам (коэффициент седиментации 7S) является единственной фракцией иммуноглобулинов, способной к транспорту через плацентарный барьер и тем самым обеспечивающей иммунитет плода и новорождённого. В составе IgG 2-3 % углеводов; два антигенсвязывающих Fab-фрагмента и один FC-фрагмент. Fab-фрагмент (50-52 кДа) состоит из целой L-цепи и N-концевой половины H-цепи, соединённых между собой дисульфидной связью, тогда как FC-фрагмент (48 кДа) образован C-концевыми половинами H-цепей. Всего в молекуле IgG 12 доменов (участки, сформированные из β-структуры и α-спиралей полипептидных цепей Ig в виде неупорядоченных образований, связанных между собой дисульфидными мостиками аминокислотных остатков внутри каждой цепи): по 4 на тяжёлых и по 2 на лёгких цепях.
- IgM (молекулярная масса 970 кДа, наиболее крупные иммуноглобулины) появляются при первичном иммунном ответе B-лимфоцитами на ранее неизвестный антиген. Составляют до 10 % фракции иммуноглобулинов. Представляют собой пентамер основной четырёхцепочечной единицы, содержащей две μ-цепи. При этом каждый пентамер содержит одну копию полипептида с J-цепью (20 кДа), который синтезируется антителообразующей клеткой и ковалентно связывается между двумя соседними FC-фрагментами иммуноглобулина. Содержат 10-12 % углеводов. Образование IgM происходит ещё в пре-B-лимфоцитах, в которых первично синтезируются из μ-цепи; синтез лёгких цепей в пре-B-клетках обеспечивает их связывание с μ-цепями, в результате образуются функционально активные IgM, которые встраиваются в поверхностные структуры плазматической мембраны, выполняя роль антиген-распознающего рецептора; с этого момента клетки пре-B-лимфоцитов становятся зрелыми и способны участвовать в иммунном ответе.
- IgA (молекулярная масса 500 кДа). Основной функцией IgA является защита слизистых оболочек дыхательных, мочеполовых путей и желудочно-кишечного тракта от инфекций. Синтезируются в основном плазматическими клетками слизистых оболочек в ответ на местное воздействие антигена. Время их полужизни — 6-7 суток. В организме человека IgA существует в двух формах — сывороточной и секреторной. Секреторный IgA представлен в димерной форме в комплексе с секреторным компонентом, содержится в серозно-слизистых секретах (например в слюне, слезах, молозиве, молоке, отделяемом слизистой оболочки мочеполовой и респираторной системы). Сывороточный IgA составляет 15-20 % всей фракции иммуноглобулинов, при этом 80 % молекул IgA представлено в мономерной форме у человека. Содержит 10-12 % углеводов.
- IgD (молекулярная масса 175 кДа) составляет менее одного процента фракции иммуноглобулинов плазмы, содержится в основном на мембране некоторых В-лимфоцитов. Функции до конца не выяснены, предположительно является антигенным рецептором с высоким содержанием связанных с белком углеводов для В-лимфоцитов, ещё не представлявшихся антигену.
- IgE (молекулярная масса 200 кДа) в свободном виде в плазме почти отсутствует. Способен осуществлять защитную функцию в организме от действия паразитарных инфекций, обуславливает многие аллергические реакции. Механизм действия IgE проявляется через связывание с высоким сродством (10 −10 М) с поверхностными структурами базофилов и тучных клеток, с последующим присоединением к ним антигена, вызывая дегрануляцию и выброс в кровь высоко активных аминов (гистамина и серотонина — медиаторов воспаления), на чём основано применение аллергических диагностических проб.
- IgY обнаружены в крови кур и яичном желтке.
По мере созревания В-клетки переключаются от синтеза IgM и IgD на синтез IgG, IgA, IgE (при этом у клеток сохраняется способность синтезировать также IgM и IgD — вплоть до трёх классов одновременно). При переключении синтеза изотипов антигенная специфичность антител сохраняется.
Какие органы участвуют в образовании антител
Основными органами, благодаря которым происходит защита организма, являются селезенка, тимус и лимфа узлы. Именно в лимфоузлах происходит образование B-лимфоцитов. Также в периферических лимфоидных структурах образуются макрофаги и T-лимфоузлы, которые также помогают образованию антител.
Макрофаги являются поисковиками антигена. Когда они его находят, то ведут его к лимфоцитам для распознания.
T-лимфоциты бывают нескольких видом. T-киллеры являются уничтожителями клеток мутантов, опухолевых клеток, а также клеток ткани трансплантата.
T-угнетаторы способны приостанавливать слишком быстрое развитие антител, приостанавливая реакцию B-лимфоцитов. Тем самым они контролируют слаженную работу иммунной системы.
T-хелперы помогают B-лимфоцитам в процессе синтеза антител. Именно этот вид лимфоцитов способствует ускорению выработки антител, или иммуноглобулина.
Антитела (иммуноглобулины, ИГ, Ig) — вид белковых соединений плазмы крови, синтезирующихся плазматическими клетками в организме человека и других теплокровных животных в ответ на попадание в него чужеродных или потенциально опасных веществ (это молекулы из бактерий или вирусов, белковые токсины и т.п вещества, которые в соответствии с их ролью в имунном ответе называют антигенами). Для каждого антигена из В-лимфоцитов формируются соответствующие ему специализировавшиеся плазматические клетки, вырабатывающие специфичные для этого антигена антитела. Антитела прикрепляются к антигенам, связываясь с определённым эпитопом — характерным фрагментом поверхности или линейной аминокислотной цепи антигена. Антитела выполняют две функции: антиген-связывающую, то есть прямо мешают антигену приносить вред, и эффекторную, то есть вызывают тот или иной иммунный ответ, например, запускают классическую схему активации комплемента.
3.1 Антитела
Антитела
— иммуноглобулины, продуцируемые
В-лимфоцитами (плазматическими клетками).
Мономеры иммуноглобулинов состоят из
двух тяжелых (Н-цепи) и двух легких
(L-цепи) полипептидных цепей, связанных
дисульфидной связью. Эти цепи имеют
константные (С) и вариабельные (V) участки.
Папаин расщепляет молекулу иммуноглобулина
на два одинаковых антигенсвязывающих
фрагмента — Fab
(Fragment anligen binding) и Fc
(Fragmenl crislalhzable). По типу тяжелой цепи
различают 5 классов иммуноглобулинов
IgG, IgM, IgA, IgD, IgE.
Они
состоят из полипептидных цепей. В
молекуле иммуноглобулина различают
четыре структуры:
1) первичную
– это последовательность определенных
аминокислот. Она строится из нуклеотидных
триплетов, генетически детерминируется
и определяет основные последующие
структурные особенности;
2) вторичную
(определяется конформацией полипептидных
цепей);
3) третичную
(определяет характер расположения
отдельных участков цепи, создающих
пространственную картину);
4) четвертичную.
Из четырех полипептидных цепей возникает
биологически активный комплекс. Цепи
попарно имеют одинаковую структуру.
Большинство
молекул иммуноглобулинов составлено
из двух тяжелых (H) цепей и двух легких
(L) цепей, соединенных дисульфидными
связями. Легкие цепи состоят или из двух
k-цепей, или из двух l-цепей. Тяжелые цепи
могут быть одного из пяти классов (IgA,
IgG, IgM, IgD и IgE).
Каждая
цепь имеет два участка:
1) постоянный.
Остается постоянным в последовательности
аминокислот и антигенности в пределах
данного класса иммуноглобулинов;
2) вариабельный.
Характеризуется большой непостоянностью
последовательности аминокислот; в этой
части цепи происходит реакция соединения
с антигеном.
Каждая
молекула IgG состоит из двух соединенных
цепей, концы которых формируют два
антигенсвязывающих участка. На
вариабельном участке каждой цепи имеются
гипервариабельные участки: три в легких
цепях и четыре в тяжелых. Разновидности
последовательности аминокислот в этих
гипервариабельных участках определяют
специфичность антитела. При определенных
условиях эти гипервариабельные области
могут также выступать в роли антигенов
(идиотипов).
В
молекуле иммуноглобулина меньше двух
антигенсвязывающих центров быть не
может, но один может быть завернут внутрь
молекулы – это неполное антитело. Оно
блокирует антиген, и тот не может
связаться с полными антителами.
При
энзиматическом расщеплении иммуноглобулинов
образуются следующие фрагменты:
1) Fc-фрагмент
содержит участки обеих постоянных
частей; не обладает свойством антитела,
но имеет сродство с комплементом;
2) Fab-фрагмент
содержит легкую и часть тяжелой цепи с
одним антигенсвязывающим участком;
обладает свойством антитела;
3) F(ab)Т2-фрагмент
состоит из двух связанных между собой
Fab-фрагментов.
Другие
классы иммуноглобулинов имеют такую
же основную структуру. Исключение –
IgM: является пентамером (состоит из пяти
основных единиц, связанных в области
Fc-концов), а IgA – димер.
Что означает снижение числа антител для образования коллективного иммунитета?
Коллективный иммунитет относится к популяции и возникает, когда достаточно большое число людей в сообществе невосприимчивы к вирусу и неспособны его передавать. Это обеспечивает защиту для тех, кто все еще уязвим. Например, если 60% людей защищены от COVID-19, потому что они подверглись инфицированию и выработали антитела, — это может защитить (через менее частые взаимодействия) оставшиеся 40% людей от заболевания.
Но исследования, опубликованные в вышеупомянутом медицинском журнале, предполагают, что люди с более низким уровнем антител все еще могут переносить вирус и не иметь никаких симптомов заболевания.
Это означает, что если такие люди с низким уровнем антител окружают здоровых, неинфицированных людей, они представляют опасность для них, потому что они могут передавать вирус.
Фото Ильи Репина
История изучения
Самое первое антитело было обнаружено Берингом и Китазато в 1890 году, однако в то время о природе обнаруженного столбнячного антитоксина, кроме его специфичности и его присутствия в сыворотке иммунного животного, ничего определённого сказать было нельзя. Только с 1937 года — исследований Тиселиуса и Кабата, началось изучение молекулярной природы антител. Авторы использовали метод электрофореза белков и продемонстрировали увеличение гамма-глобулиновой фракции сыворотки крови иммунизированных животных. Адсорбция сыворотки антигеном, который был взят для иммунизации, снижала количество белка в данной фракции до уровня интактных животных.
История изучения
Самое первое антитело было обнаружено Берингом и Китазато в 1890 году, однако в то время о природе обнаруженного столбнячного антитоксина, кроме его специфичности и его присутствия в сыворотке иммунного животного, ничего определённого сказать было нельзя. Только с 1937 года — исследований Тиселиуса и Кабата, началось изучение молекулярной природы антител. Авторы использовали метод электрофореза белков и продемонстрировали увеличение гамма-глобулиновой фракции сыворотки крови иммунизированных животных. Адсорбция сыворотки антигеном, который был взят для иммунизации, снижала количество белка в данной фракции до уровня интактных животных.
Антитела при беременности
При обращении женщины в женскую консультацию при становлении на учет по беременности ей обязательно назначают прохождение анализа крови на антитела. При этом изучается не только наличие у нее в крови антител к разного рода вирусным заболеваниям, но также и уточняется резус-фактор
.
Такая процедура особенно важная для женщин, имеющих резус-отрицательный фактор крови. Если у отца ребенка резус положительный, то при наследовании плодом генов отца может произойти резус-конфликт. Это состояние при котором антитела в крови матери начинают отторгать плод, как чужеродный организм
. При этом может наступить выкидыш и отслоение плаценты.
И также обязательно проводится проверка беременной женщины на антитела к краснухе
. Это заболевание крайне опасно для плода и для самой беременной. Вирус краснухи способен внедряться в ткани плода и вызывать пороки развития и нарушения в формировании внутренних органов. Поэтому если женщина планирует беременность, то врачи рекомендуют ей заблаговременно сделать прививку от краснухи.
Если же беременность уже наступила, то по анализу крови на антитела врач выявляет вероятность заражения будущей матери краснухой. Для этого проводится проверка антител IgM и IgG
.
Если результаты показывают «IgM –, IgG +», то значит, что женщина уже переболела краснухой и у нее в крови присутствуют антитела, способные противостоять заболеванию, следовательно, ребенку ничто не угрожает.
Если же результаты анализа указывают на положительный IgM, то отсюда следует что беременная женщина уже больна как минимум в течение двух месяцев. В этом случае врачи предлагают ей провести аборт по медицинским показаниям
.
Ответы на частые вопросы
Какой титр антител к коронавирусу считается высоким? Четкие количественные критерии для систем тестирования на антитела к коронавирусной инфекции пока не выработаны. На данном этапе во всем мире осуществляется сбор и накопление сведений о новом коронавирусе, в том числе данных о его лабораторной диагностике методом ИФА. Поэтому невозможно сказать, какой именно титр антител к нему может считаться достоверно высоким. По словам Ивана Скороходова, члена ассоциации аллергологов и иммунологов России, человек, переболевший коронавирусом, может стать донором плазмы для тяжелых больных, если показатели IgG у него будут достаточно высокими
Для этого важно проконтролировать условия: титр IgG должен быть больше 40, а IgM больше или равно 1,5, или же титр IgG больше 80, а IgM больше или равен нулю
Какой титр антител указывает на то, что у человека сформировался иммунитет к коронавирусу? Чтобы сформировался иммунитет к COVID-19, показатель иммуноглобулинов IgG должен быть больше 10. Но даже если по результатам анализа обнаружены иммуноглобулины IgG в таком количестве, нельзя утверждать, что человек будет обладать стойким иммунитетом к COVID.
Максимальный уровень иммуноглобулинов класса G наблюдается спустя два-три месяца после заражения. Но клинические исследования показали, что у большинства людей, заразившихся коронавирусом, защитный титр антител существенно снижается уже через три месяца после перенесенного заболевания. А у тех, кто страдает сахарным диабетом, ожирением, аллергическими и аутоиммунными заболеваниями, титр иммуноглобулинов G начинает снижаться еще раньше – через два месяца после перенесенного заболевания. В частности, по данным ученых из Королевского колледжа Лондона, антитела к коронавирусу сохранились лишь у 17% переболевших им. Можно лишь предположить, что иммунитет к коронавирусу кратковременный. Чтобы установить, насколько стойкий иммунитет после перенесенной коронавирусной инфекции, необходимы углубленные иммунологические исследования.
Какой титр антител к коронавирусу считается достаточным? По причине отсутствия точных данных, подтвержденных клиническими исследованиями, нельзя говорить и о достаточном для дальнейшей защиты от повторного заражения титре антител к коронавирусу. Основываясь на общих закономерностях, характерных для вирусных инфекций, напрашивается вывод, что после перенесенной инфекции при повторном заражении иммунная система формирует антитела быстрее. Это значит, что при повторном инфицировании болезнь будет протекать легче.
На заметку: Считается, что результаты иммуноферментного анализа отличаются высокой точностью, но иногда (например, при перекрестной реакции с другими коронавирусами) анализ может показать ложноположительный результат. Ложноотрицательные результаты возникают и из-за недостаточной чувствительности теста. Во всех сомнительных случаях обязательно ПЦР-тестирование.
Какие показания для проведения диагностики COVID-19 с помощью ИФА?
Сдать кровь на антитела к коронавирусу необходимо в следующих случаях:
- для диагностирования активной стадии заболевания при наличии респираторных симптомов;
- для исключения заражения при установленном контакте с заболевшим;
- для уточнения диагноза заболевания при слабо выраженной симптоматике;
- для диагностики скрытых форм (носительства) коронавирусной инфекции;
- для того чтобы узнать, переболел ли человек COVID-19 и сформировался ли у него иммунитет к коронавирусу, в том числе при бессимптомном течении заболевания;
- при отборе донора для переливания крови пациентам с тяжелым течением коронавирусной инфекции.
Какими бывают защитные барьеры организма
Все многоклеточные организмы, и человек в том числе, подвергаются непрерывным атакам со стороны бактерий, вирусов и паразитов. Первый барьер на их пути – это кожа и слизистые оболочки, создающие не только физическую преграду, но и выделяющие губительные для микробов секреты (пот, кожное сало). Обезвреживать патогенные микроорганизмы способны также соляная кислота, слюна, слезы и ряд других веществ, выделяемых слизистыми покровами.
Второй барьер на пути болезнетворных микроорганизмов осуществляют внутренние среды организма: кровь, лимфа, тканевая жидкость. Способность организма избавляться от чужеродных тел и соединений и сохранять тем самым постоянство внутренней среды называется иммунитетом.
Лекция 3 Генетическая основа разнообразия специфичности активных центров антител
Первая теория разнообразия специфичности
антител была разработана П.Эрлихом в
начале ХХ в. Это «Теория боковых цепей».
Согласно теории Эрлиха, на поверхности
клеток изначально присутствует множество
разнообразных белковых молекул, «боковых
цепей», каждая из которых способна
связываться с определенным антигеном.
В случае попадания антигена в организм,
его молекулы соединяются с определенным
рецептором и отрывают его от мембраны.
В ответ на это клетка реагирует усиленной
продукцией именно этого рецептора и,
таким образом, происходит компенсаторное
увеличение количества требуемых для
нейтрализации данного антигена антител.
Следующая теория специфичности
антител принадлежит Гауровитцу. Она
называется «Матричная теория». Согласно
теории Гауровитца, после попадания
антигена внутрь клетки, он служит в
качестве матрицы, на которой происходит
формирование активного центра антитела.
В 70-80-х годах ХХ в. было показано,
что в основе разнообразия специфичности
активных центров антител лежит особенность
строения генов, кодирующих вариабельные
области тяжелых и легких цепей.
Гены легкой цепей расположены на
22-й хромосоме. Вариабельный участок
легкой цепи представлен 250 вариантами
генов V, расположенных
последовательно друг за другом. Далее
расположены несколько вариантов генаJ, после которого находятся
гены константной области (гены С). В
процессе созревания В-лимфоцитов
случайным образом происходит выпадение
(делеция) частиV– генов
и рядом оказываются один изV-генов
и генJ. Образуется
последовательностьVnJnC,
которая и обусловливает структуру
легкой цепи. Таким образом, в В-лимфоците
возможно образование одного из 2000
вариантов строения вариабельной области
легкой цепи.
Гены тяжелых цепей иммуноглобулинов
расположены на 14-й хромосоме. Они включают
группу генов вариабельной области (V),
дополнительный участок (D),
соединительные гены -Jи
гены константной области – С. Таким
образом, последовательность генов,
кодирующих тяжелые цепи, представлена
в следующем порядке:VDJC.
В результате рекомбинаций, которые
происходят в процессе созревания
В-лимфоцитов, возможно образование
120000 вариантов последовательностейVDJC, которая и определяет
строение вариабельного участка тяжелой
цепи.
Учитывая , что активный центр антитела
строится из вариабельных доменов тяжелой
и легкой цепи, общее число возможных
конфигураций активного центра антител
достигает 2,4х108. Данная цифра
указывает на количество клонов
В-лимфоцитов, обладающих разным строением
активного центра, т.е. разной специфичностью.
Какие бывают антитела к щитовидке и почему они появляются
Идентификация и уничтожение чужеродных агентов – основная функция иммунной системы. При попадании в организм бактерий, вирусов или грибков иммунные клетки начинают синтезировать антитела – специфические иммуноглобулины, уничтожающие опасные вещества. Но если система дает сбой, в крови образуются аутоантитела против собственных органов или тканей.
В эндокринологии выделяют 3 типа иммуноглобулинов щитовидной железы. Они вырабатываются против:
- тиреоглобулина (антиТГ);
- тиреопероксидазы (антиТПО);
- рецепторов ТТГ (анти-рТТГ).
Антитела (АТ) железы присутствуют в организме здорового человека в малых количествах. Если их концентрация превышает референсные (нормальные) значения, это указывает на аутоиммунные патологии.
АнтиТГ
Антитела к тиреоглобулину – иммуноглобулины, которые вырабатываются против предшественника тиреоидных гормонов. Тиреоглобулин относится к гликопептидам. Он синтезируется фолликулами щитовидной железы, из него далее получаются основные гормоны:
- трийодтиронин (Т3);
- тироксин (Т4).
По неизвестным причинам тиреоглобулин начинает восприниматься иммунной системой как чужеродный объект. В ответ к нему синтезируются аутоантитела, вследствие чего в железе возникает воспаление. Высокий уровень антител к ТГ является точным показателем аутоиммунных патологий у женщин и мужчин – тиреоидита Хашимото, Базедовой болезни.
АнтиТПО
Антитела к тиреопероксидазе вырабатываются против фермента железы, отвечающего за синтез активной формы йода, необходимого для продукции Т3 и Т4. Они образуются, когда иммунитет идентифицирует функциональную (тиреоидную) ткань железы как инородное тело.
Аутоантитела бомбардируют щитовидку, что приводит к воспалению. Без должного лечения количество тироцитов – функциональных клеток – уменьшается, что становится причиной гипотиреоза. Отклонение антиТПО (АТ-ТПО) от нормы – один из признаков диффузного токсического зоба, врожденного гипотиреоза, тиреоидита Хашимото.
Анти-рТТГ
Антитела к рецепторам ТТГ – иммуноглобулины, которые взаимодействуют с рецепторами щитовидки, чувствительными к тиреотропину (ТТГ). В зависимости от принципа действия различают 2 типа анти-рТТГ:
- Блокирующие – угнетают функцию железы за счет уменьшения чувствительности рецепторов к тиреотропину, который синтезируется аденогипофизом (передней долей гипофиза). Они провоцируют истощение тиреоидной ткани железы, что приводит к ее недостаточности и гипотиреозу.
- Стимулирующие – увеличивают чувствительность клеток-мишеней к тиреотропину, что приводит к гиперактивности железы. В результате уровень Т3 и Т4 многократно увеличивается, из-за чего возникает гипертиреоз и токсический зоб.
Для выявления специфических иммуноглобулинов, определения их типа и концентрации назначают иммуноферментный анализ крови.
- радиационное облучение;
- хронические инфекции;
- генетическая предрасположенность;
- сахарный диабет;
- хроническое отравление токсинами;
- йододефицитные состояния.
По статистике, патологии железы в 3 раза чаще диагностируются у женщин. Это связано с гормональным дисбалансом на фоне циклического увеличения и уменьшения стероидных гормонов.
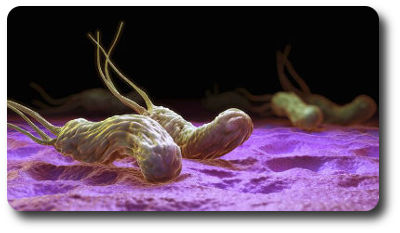
Антитела к бактерии Helicobacter pylori
Хеликобактер содержится «на правах постоянного проживания» в желудке и двенадцатиперстной кишке у 70% взрослого населения. Как только появляются нарушения в питании, учащаются стрессовые ситуации, происходит прием алкоголя, инфекция активизируется и становится возбудителем воспалительного процесса от простого гастрита до язвенной болезни. Длительное поражающее действие бактерии провоцирует развитие раковой опухоли.
Хеликобактерии за работой: уничтожают клетки эпителия
Анализ проводят при наличии симптомов нарушения пищеварения (боли, непереносимость пищи, тошнота, изжога), для оценки эффективности проведенного лечения, в качестве профилактики язвенной болезни.
О наличии Хеликобактер говорит сочетание трех классов антител:
- IgA и IgM обнаруживается уже в ранних стадиях заражения;
- IgG появляется только через месяц, поэтому, если в первых анализах результат отрицательный, то это пока ни о чем не говорит, следует повторить его через четыре недели.
Память иммунной системы
История воздействия патогена на организм «записывается» в так называемых Т-клетках памяти и В-клетках памяти. Эти клетки располагаются в периферических тканях организма, таких как лимфатические узлы или селезенка, и служат памятью о болезнетворном вирусе после того, как инфекция побеждена и уже исчезла. Такая иммунологическая память отвечает за защиту организма и вступает в действие в случае второй волны или атаки патогена.
Это нормально, когда уровень антител снижается после того, как человек выздоровел от болезни. Но статья в New England Journal of Medicine вызвала беспокойство, потому что она предполагает, что мы теряем нашу иммунологическую память, что в свою очередь так же плохо, как потеря реальной памяти.
Диагностика туберкулеза

На рентгеновских снимках хорошо видно туберкулез легких на более поздних стадиях. Однако для выявления внелегочной формы или ранней степени туберкулеза проводят анализ крови на АТ к палочке Коха.
Самым информативным методом исследования является реакция Манту. Пациенту подкожно вводят туберкулин и оценивают кожную реакцию. Не всегда сильная реакция свидетельствует о болезни. Это может быть признаком того, что человек столкнулся с бактериями, но его иммунитет смог их побороть. Также ложноположительный результат может быть при аллергической реакции на вакцину.
Для более точных результатов проводят дополнительно диаскин тест.
Вариабельность антител
Антитела являются чрезвычайно вариабельными (в организме одного человека может существовать до 108 вариантов антител). Всё разнообразие антител проистекает из вариабельности как тяжёлых цепей, так и лёгких цепей.
У антител, вырабатываемых тем или иным организмом в ответ на те или иные антигены, выделяют:
- Изотипическая вариабельность — проявляется в наличии классов антител (изотипов), различающихся по строению тяжёлых цепей и олигомерностью, вырабатываемых всеми организмами данного вида;
- Аллотипическая вариабельность — проявляется на индивидуальном уровне в пределах данного вида в виде вариабельности аллелей иммуноглобулинов — является генетически детерминированным отличием данного организма от другого;
- Идиотипическая вариабельность — проявляется в различии аминокислотного состава антиген-связывающего участка. Это касается вариабельных и гипервариабельных доменов тяжёлой и лёгкой цепей, непосредственно контактирующих с антигеном.