Заболевание вильсона-коновалова
Содержание:
Клиническая картина и течение
Гепато-церебральная дистрофия начинается в детском или молодом возрасте и имеет хроническое прогрессирующее течение. Во многих случаях появлению симптомов поражения нервной системы предшествуют висцеральные расстройства в виде нарушения деятельности печени и желудочно-кишечных расстройств (желтуха, боли в правом подреберье, диспептические явления). Порой развивается выраженный гепато-лиенальный синдром. Со стороны нервной системы на первый план выступают экстрапирамидные симптомы в виде мышечной ригидности, гиперкинезов и расстройств психики. Пирамидные симптомы могут быть, но чаще отсутствуют. Чувствительность обычно не нарушена.
Типичным симптомом болезни являются кольца Кайзера-Флейшера — отложения по периферии роговой оболочки содержащего медь зеленовато-бурого пигмента, более выраженные на поздних стадиях. Иногда отмечается желтовато-коричневая пигментация кожи туловища и лица. Часты геморрагические явления (кровоточивость дёсен, носовые кровотечения, положительная проба жгута), мраморность кожи, акроцианоз. Капилляроскопия обнаруживает атонию капилляров и застойность кровотока. Отмечаются суставные боли, профузные поты, остеопороз, ломкость костей.
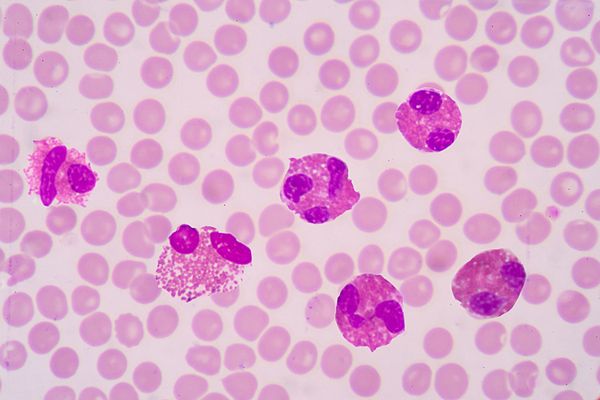
Патология печени клинически выявляется примерно у 30 % больных, а в ряде случаев она может быть обнаружена только функциональными пробами, например пробой с нагрузкой галактозой, пробой Квинка, пробой Бергмана-Эльботта, бромсульфофталеиновой пробой; количество билирубина в крови и уробилина в моче обычно увеличено; изменены осадочные реакции Таката-Ара и Грея, обычны лейкопения, тромбоцитопения, гипохромная анемия.
Различают 5 форм гепато-церебральной дистрофии:[уточнить]
- Брюшная форма — тяжёлое поражение печени, приводящее к смерти раньше появления симптомов со стороны нервной системы; заболевают дети. Её продолжительность от нескольких месяцев до 3-5 лет.
- Ригидно-аритмогиперкинетическая, или ранняя форма — отличается быстрым течением; начинается также в детском возрасте. В клинической картине преобладают мышечная ригидность, приводящая к контрактурам, бедность и замедленность движений, хореоатетоидные или торсионные насильственные движения. Характерны дизартрия и дисфагия, судорожный смех и плач, аффективные расстройства и умеренное снижение интеллекта. Заболевание длится 2-3 года, заканчивается летально.
- Дрожательно-ригидная форма встречается чаще других; начинается в юношеском возрасте, течёт медленнее, порой с ремиссиями и внезапными ухудшениями, сопровождающимися субфебрильной температурой; характеризуется одновременным развитием тяжёлой ригидности и дрожания, дрожание очень ритмичное (2-8 дрожаний в секунду), резко усиливается при статическом напряжении мышц, движениях и волнении, в покое и во сне исчезает. Иногда обнаруживаются атетоидные хореоформные насильственные движения; наблюдаются также дисфагия и дизартрия. Средняя продолжительность жизни около шести лет.
- Дрожательная форма начинается в возрасте 20-30 лет, течёт довольно медленно(10-15 лет и больше); дрожание резко преобладает, ригидность появляется лишь в конце болезни, а порой наблюдается гипотония мышц; отмечается амимия, медленная монотонная речь, тяжёлые изменения психики, часты аффективные вспышки. Наблюдаются эпилептиформные припадки.
- Экстрапирамидно-корковая форма встречается реже других форм. Типичные для гепато-церебральной дистрофии нарушения в дальнейшем осложняются апоплектиформно развивающимися пирамидными парезами, эпилептиформными припадками и тяжёлым слабоумием (обнаруживаются обширные размягчения в коре больших полушарий). Длится 6-8 лет, заканчивается летально.
Наибольшая летальность (50 %) отмечается при печёночной форме с массивным некрозом и гемолизом у детей до 6 лет. Смерть больных от неврологических нарушений при отсутствии лечения наступает через 5-14 лет. Основная причина при этом интеркуррентные заболевания или желудочно-кишечные кровотечения, портальная гипертензия.
Диагностика болезни Вильсона
Очень важно, чтобы болезнь Вильсона была диагностирована своевременно. Чем раньше будет поставлен диагноз и начато лечение, тем менее выраженными будут поражения печени, головного мозга и других структур организма
Диагностика болезни Вильсона может быть довольно затруднительной. При этом заболевании у человека развивается печеночная недостаточность неизвестной этиологии. Часто своевременно не удается установить причину заболевания. На начальных этапах Болезнь Вильсона-Коновалова проявляется только повышением уровня печеночных ферментов, выявляемое при биохимическом анализе крови.
Диагностируется болезнь Вильсона на основании ряда исследований:
- Лабораторное исследование крови. При циррозе печени общий анализ крови показывает анемию, недостаток лейкоцитов и тромбоцитов. Также у больного нарушается свертываемость крови.
- Проводят также биохимическое исследование крови. У людей с болезнью Вильсона-Коновалова наблюдают повышение уровня активности печеночных ферментов, а также нарушение нормы почечных показателей.
- Также определяют концентрацию белка церулоплазмина в сыворотке крови. У большинства больных концентрация этого протеина снижается. Дополнительно проводят определение концентрации самой меди в сыворотке. Поскольку 95% меди содержится в сыворотке именно в составе белка церулоплазмина, то содержание этого металла в сыворотке крови у больных с болезнью Вильсона-Коновалова также снижено.
- Лабораторное исследование мочи. У больных с печеночной недостаточностью нарушается работа почек, что проявляется патологическими изменениями характеристик мочи.
- Определение экскреции меди с мочой. У людей с болезнью Вильсона наблюдают усиление выведения меди с мочой. У здоровых людей экскреция меди составляет в среднем 30-40 мкг/сут., но не превышает 50 мкг/сут. При болезни Вильсона-Коновалова этот показатель может превышать 100 мкг/сут., а у больных с печеночной недостаточностью доходить до 1000 мкг/сут. Однако у некоторых больных этот показатель не повышается.
- Генетический анализ. С помощью этого метода можно определить наличие в организме человека одной из мутаций гена АТР7В.
- Инструментальная диагностика. Эти диагностические процедуры показывают патологические изменения внутренних органов, вызванные накоплением меди. Проводят электрокардиографичекое исследование работы сердца; ультразвуковое исследование органов брюшной полости, которое выявляет цирроз печени, наличие асцита в брюшной полости; электроэнцефалография выявляет нарушения проводимости нейронов головного мозга, склонность к эпилептическим припадкам; рентгенологическое исследование костей, выявление очагов пониженной плотности костной ткани, остеопороза; компьютерная и магнитно-резонансная томография головного мозга и органов брюшной полости.
- Биопсия и морфологическое исследование печени показывает дистрофические изменения ткани печени. Также проводят определение концентрации меди в пересчете на грамм сухого вещества. Офтальмологическое обследование выявляет накопление меди в роговице глаза.
Причины болезни Вильсона-Коновалова
Медь является очень важным микроэлементом. Она используется в синтезе некоторых ферментов, и без нее организм не может выполнять ряд обменных процессов. Вместе с тем, купрум – это тяжелый металл, избыток которого вызывает токсическое поражение клеток. Накопление этого металла приводит к тяжелым последствиям: развивается печеночная и почечная недостаточность, нарушается работа нервной системы.
Перенос ионов меди осуществляется при помощи специального белка АТФ-азного протеина Р-типа. Этот протеин связывает металл и присоединяет к другим белкам. Кодирует АТФ-азный булок Р-типа ген АТР7В, который размещен на одной из аутосом. Мутации в этом гене приводят к сбоям в синтезе белкового продукта. В результате получается неполноценный протеин, не способный в полной мере выполнять свои функции, и возникают нарушения транспорта меди. Известно порядка двух сотен мутаций, которые могут к этому привести.
Болезнь Вильсона – это наследственное заболевание. Оно возникает при наследовании детьми мутантного аллеля АТР7В гена, который ответственен за обмен меди. Этот ген наследуется по аутосомно-рецессивному типу.
Что такое аутосомно-рецессивное наследование? Гены упакованы в пары хромосом. Всего их 46, то есть 23 пары: 22 пары аутосом и 1 пара половых хромосом. Если у гена аутосомный тип наследования, это значит, что он локализован на одной из аутосом, и наследование такого гена не связано с полом. То есть, болезнь Вильсона-Коновалова может наследоваться с равной вероятностью мальчиками и девочками. Из двух хромосом одной пары одна достается ребенку от мамы, а вторая – от папы. Каждая хромосома содержит одинаковый набор генов, ответственных за тот или иной признак. Каждый ген может быть представлен доминантным или рецессивным аллелем. Доминантный аллель всегда проявляется, в то время как рецессивный в паре с доминантным всегда скрыт скрыт. Если в организме человека содержится два доминантных или два рецессивных аллеля одного гена, то он считается гомозиготным по данному признаку, а если один доминантный и один рецессивный – то гетерозиготным. В случае гетерозиготы проявится только доминантный ген, а рецессивный будет скрыт.
Дефектный ген, который приводит к развитию болезни Вильсона, является рецессивным. Это означает, что он может никак не проявляться у родителей, но вызвать болезнь у их детей. Если мама и папа были гетерозиготами по данному признаку, и в геноме каждого из них был скрыт мутантный аллель гена, то у них может родиться ребенок, который унаследует оба рецессивных гена от обоих родителей. У такого ребенка проявится болезнь Вильсона-Коновалова. Вероятность этого события составляет 25%.
Еще 50% вероятности составляет то, что у таких родителей родятся дети-носители рецессивного дефектного гена, которые унаследуют его от одного из родителей. От второго родителя эти дети унаследуют доминантный нормальный ген. У таких детей не возникнет нарушение обмена меди, но сохраняется вероятность передачи заболевания уже своим детям.
Чаще патологии, наследуемые по аутосомно-рецессивному типу проявляются в культурах, где практикуются браки между кровными родственниками, поскольку у них вероятность наличия одного и того же рецессивного гена выше.
Классификация болезни Вильсона
Советский невропатолог Н.В. Коновалов, который занимался изучением патофизиологии, патогенеза, клиники данного заболевания, классифицировал болезнь, выделив пять ее форм:
- Брюшная: когда поражается печень, что приводит к смерти больного раньше, чем проявляются симптомы, диагностируется в детском возрасте, продолжительность — до пяти лет.
- Ригидно-аритмогиперкинетическая — быстро прогрессирующая форма, наблюдается в детском возрасте, характеризуется мышечной ригидностью, замедленностью движений, образованием контрактур, наблюдаются судорожный смех и плач, присутствует задержка в развитии.
- Дрожательная: наблюдается во взрослом возрасте (20-30 лет), прогрессирует медленно (около 10 лет), характеризуется дрожанием. На последней стадии появляется ригидность, наблюдается анемия, заторможенность и монотонность речи, тяжелая деградация психики, свойственны эпилептические припадки.
- Дрожательно-ригидная — самая распространённая форма, наблюдается в подростковом возрасте, развивается тяжелая ригидность и сильное дрожание, симптомы усиливаются при волнении или физическом напряжении мышц, сопровождается дисфагией и дизартрией, прогрессирует около шести лет.
- Экстрапирамидно-корковая — встречается редко, отягощается пирамидными парезами, эпилептическими припадками и тяжелой степенью слабоумия из-за сильного размягчения больших полушарий головного мозга.
Диагностика болезни Вильсона — Коновалова
Диагноз основывается на сочетании клинических симптомов, лабораторных данных и молекулярно-генетического тестирования. Ни один лабораторный тест, за исключением определения болезнетворного гена АТР7В на молекулярном уровне, не обеспечивает 100 % гарантию диагностики заболевания.
Основные диагностические показатели болезни Вильсона — Коновалова:
- Церулоплазмин: снижение на 50 %. Может быть нормальным. По другим данным — менее 20 мг/дл. По ряду причин (болезнь Менкеса, печёночная недостаточность, нефротический синдром, длительное парентеральное питание и др.) анализ может быть ложноотрицальным.
- Суточная экскреция меди с мочой: >100 мкг/сут., или > 40 мкг/сут. у детей. При бессимптомном течении показатели не превышают норму 40 мкг/сут.
- «Свободная» медь сыворотки: > 1,6 мкМ/л
- Медь в ткани печени: > 4 мкМ/г или > 250 мкг/г сухого веса.
| Симптомы | Лабораторные тесты |
|---|---|
| 1. Кольца Кайзера-Флейшера:• присутствуют (0 баллов)• отсутствуют (2 балла) | 1. Экскреция (выделение) меди с мочой:• норма (0 баллов)• 1-2 нормы (1 балл)• более 2 норм (2 балла)• норма, но увеличение более 5 норм при пробе с купренилом (2 балла) |
| 2.Нейропсихиатрическая симптоматика: (изменения на МРТ)• присутствует (2 балла) • отсутствует (0 баллов) | 2. Количественное определение меди в биоптатах печени:• норма (-1 балл) • 50-250 мкг/г (1 балл)• Более 250 мкг/г (2 балла) |
| 3. Кумбс-негативная гемолитическая анемия:• присутствует (1 балл) • отсутствует (0 баллов) | 3. Родамин – позитивные гепатоциты (при невозможности количественного определения меди в печени):• присутствуют (0 баллов) • отсутствуют (1 балл) |
| 4. Уровень церулоплазмина в сыворотке крови (при норме более 20 мг/дл):• норма (0 баллов) • 10-20 (1 балл) • менее 10 (2 балла) | |
| Молекулярно-генетическое исследование (выявление мутаций гена АТР7В) • гомозигота (два одинаковых гена определяющих в данном случае проявление болезни) или компаунд-гетерозигота, (из пары генов оба имеют разные мутации, приводящие к болезни, но они не идентичны друг другу) (4 балла)• гетерозигота (один ген из пары является нормальным, один с мутацией) (1 балл)• мутаций не обнаружено (0 баллов) |
Суммарные баллы:
- 4 и более — высокая вероятность болезни;
- 2-3 — болезнь вероятна, но требуется дальнейшее обследование пациента;
- 0-1 — болезнь сомнительна.
Для уточнения степени поражения и формы заболевания используются МРТ головного мозга, хотя только на основании МРТ диагноз поставить нельзя. При МРТ исследовании сразу видны характерные очаги и уменьшение объёма головного мозга. Специфичным, но более редко встречающимся симптомом при данном заболевании на МРТ снимке является картина, напоминающая «лицо гигантской панды». КТ- и МРТ-проявления могут опережать клиническую симптоматику.
Компьютерная томография (КТ) головного мозга при наличии болезни выявляет увеличение желудочков, атрофию коры и ствола мозга. Однако более важным диагностическим методом при церебральной форме заболевания является именно МРТ.
Для определения очагов скопления меди и нехирургической оценки метаболизма мозга может потребоваться магнитно-резонансная спектроскопия (МРС). Это метод, позволяющий оценить изменения биохимической концентрации веществ при различных заболеваниях в тканях организма.
Также используется позитронно-эмиссионная томография (ПЭТ), позволяющая определить степень обмена и транспорта веществ в организме.
Перспективным методом ранней диагностики является транскраниальное УЗИ головного мозга.
Изменения, определяемые при УЗИ, КТ и МРТ печени и почек определяются и при других болезненных состояниях, поэтому не являются строго специфичными для болезни Вильсона — Коновалова и могут быть использованы только для оценки эффективности лечения.
Новым методом диагностики степени выраженности цирроза (фиброза) печени является эластометрия печени. Исследование использует способность ультразвука проходить с различной скоростью через ткани разной плотности, что позволяет определить изменение нормальной плотности органа .
Причины болезни Вильсона
Болезнь Вильсона — наследственное, поддающееся лечению заболевание, при котором происходит постепенное накопление меди в печени, головном мозге (преимущественно в базальных ядрах), роговице, почках, что вызывает тяжелые функциональные нарушения, ведущие к необратимым повреждениям. Без лечения заболевание заканчивается смертью, однако своевременная постановка диагноза и лечение устраняют или предотвращают его симптомы.
Болезнь Вильсона наследуется аутосомно-рецессивно. Распространенность гетерозигот по мутантному гену составляет 1:200, а гомозигот — 1:30 000. Ген, ответственный за болезнь Вильсона, расположен на 13-й хромосоме вблизи гена, кодирующего эстеразу D. У 95% больных наблюдается дефицит или полное отсутствие церулоплазмина (сывороточный белок, играющий главную роль в транспорте меди). Это обусловлено снижением транскрипции гена церулоплазмина, расположенного на 3-й хромосоме.
Медь (Cu) — важнейший микроэлемент, который входит в состав ферментов, например цитохромоксидазы, тирозиназы, супероксиддисмутазы и др.
Метаболизм меди. Поступление Cu в организм в норме составляет приблизительно 2-5 мг в сутки, из которых 40-60 % всасываются в желудке и верхнем отделе двенадцатиперстной кишки. С помощью переносчика Си поступает в клетки печени, связывается с белками или включается в состав церулоплазмина (ферроксидаза), который относительно прочно связывает шесть атомов Cu. В комплексе с церулоплазмином Cu выделяется в плазму (приблизительно 93 % от содержания в плазме), где она окисляет Fe2+ в Fe3+. Незначительное количество Cu, связанное с церулоплазмином, высвобождается в периферических тканях. Экскреция Cu в желчь осуществляется с помощью АТФазы Р-типа, которая называется Cu-АТФаза (АТР7В). «Состарившийся», не содержащий сиаловых кислот церулоплазмин разрушается в печени, Си высвобождается, прочно связывается с белками желчи и выводится из организма с калом. В сутки выделяется приблизительно 1,2 мг меди.
Болезнь Вильсона (гепатолентикулярная дегенерация) — аутосомно-рецессивное нарушение метаболизма Cu, при котором в печени, ЦНС, глазах и других органах происходит ее избыточное отложение. Заболевание вызывается мутациями гена АТР7В, кодирующего белок CU-ATP7B. Мутация приводит к снижению выведения значительного количества Cu с желчью и уменьшению включения Cu в церулоплазмин. В результате при общей концентрации Си ниже нормы в печени и затем в плазме накапливается свободная или слабо связанная медь. В такой форме Cu токсична, поскольку связывается преимущественно с сульфгидрильными группами белков и способствует образованию свободных радикалов O2 и перекисному окислению липидов.
Накопление свободной Cu вызывает развитие анемии и хронического гепатита, который впоследствии приводит к циррозу. При молниеносном гепатите из некротически измененной ткани печени внезапно высвобождается большое количество Cu, что может вызвать гемолитический криз. Накопление Cu в ЦНС приводит к многочисленным и разнообразным неврологическим, нервно-мышечным и психогенным расстройствам. Отложение Cu в виде зернистой массы в десцеметовой оболочке глаз способствует образованию кольца Кайзера—Флейшера по периферии роговицы. В патологический процесс могут вовлекаться почки, скелет и сердце. Поскольку избыточное отложение Си обусловлено мутацией гена АТР7В, излечение от болезни Вильсона возможно путем трансплантации печени.
Диагностика
Исследование плазмы больного гепатоцеребральной дистрофией выявляет нарушения метаболизма меди. Анализ крови при гепатоцеребральной дистрофии выявляет уменьшение количества общей меди и понижение уровня церулоплазмина (ферроксидаза, содержащая медь). Исследование пробы крови делают для выявления маркеров, указывающих на вирусный гепатит. Основанием для подтверждения болезни Вильсона-Коновалова у взрослых пациентов являются диагностические критерии:
- Увеличение количества меди, находящейся в свободном состоянии в сыворотке крови.
- Усиление экскреции (выделения) меди с мочой.
- Присутствие кольца Кайзера-Флейшера (ободки золотистого или зелено-золотистого оттенка вокруг роговой оболочки). Симптом обнаруживается в ходе офтальмологического осмотра при помощи щелевой лампы.
- Увеличение количества меди в печеночных биоптатах (материал, полученный в ходе биопсии).
- Наличие отложений меди в веществе головного мозга (признак обнаруживается в ходе исследования КТ, МРТ).
- Генные мутации, типичные для БВК (по результатам генетического исследования).

Дифференциальная диагностика при болезни Вильсона-Коновалова проводится в отношении заболеваний, которые протекают с подобными клиническими проявлениями. Биохимические печеночные пробы при таких заболеваниях, как вирусный гепатит, протекающий в хронической форме, гепатит, коррелирующий с аутоиммунными нарушениями, характерны для БВК.
Аналогичная симптоматика наблюдается при билиарном циррозе (болезнь печени аутоиммунного генеза, сопровождающаяся холестазом), токсическом повреждении тканей печени, болезни печени, связанные с алкогольным и неалкогольным (жировым) поражением тканей. Дифференциальная диагностика при неврологической форме проводится в отношении болезни Паркинсона, (доброкачественное, чаще наследственное дрожание голосовых связок, головы, рук и других частей тела).
Аналогичная неврологическая симптоматика характерна для наследственных форм атаксии (нарушение согласованности при движении, совершаемом группой мышц) и дистонии (нестабильность, повышение или понижение тонуса гладкой мускулатуры кровеносных сосудов), гипертиреоидизма (гиперфункция, усиленная продукция гормонов щитовидной железы), интоксикаций фармацевтическими препаратами.
В группе риска люди, у которых имеются близкие родственники с диагностированной любой формой БВК. Показанием к диагностическому скринингу служит наличие определенных симптомов или заболеваний у людей в возрасте 5-35 лет. В числе показаний к обследованию:
- Хронические патологии печени невыясненной этиологии.
- Неврологические, психические расстройства невыясненной этиологии.
- Анемия гемолитического типа невыясненной этиологии.
- Артриты невыясненной этиологии, затрагивающие крупные суставы.
- Нарушения в работе эндокринной системы невыясненной этиологии.
- Патологии почек невыясненной этиологии.
Первичное обследование включает определение показателей церулоплазмина и меди в крови, объема меди, выделяемого вместе с мочой (в течение 24 часов), генетическое типирование (выявление мутаций гена ATP7B). УЗИ органов, расположенных в брюшной полости, показывает состояние печени, почек, селезенки, желчного пузыря и желчевыводящих путей.
Показаны консультации врачей – невролога, офтальмолога, гепатолога, гастроэнтеролога, генетика. Анализ кала (на наличие крови), исследование пробы крови, коагулограмму (показатели свертываемости крови) делают в рамках диспансерного наблюдения 1 раз на протяжении года.

Патологическая анатомия
Печень уменьшена и бугриста. Атрофический цирроз печени мало отличается от лаэннековского. Микроскопически участки печени нормального строения, чередуются с некротическими. Отмечаются и регенеративные явления, разрастание рубцовой и молодой соединительной ткани, богатой сосудами. В печени содержится большое количество зёрен меди. Изменения сосудов печени имеют большое значение в нарушении барьерной функции, так как кровь воротной вены может, минуя печень, может поступать прямо в нижнюю полую вену. Наблюдается увеличение селезёнки, гиперплазия её пульпы, явления нефрита, жировое перерождение почечного эпителия, отложение извести.
Изменения в нервной системе расцениваются как ангиотоксические и цитотоксические; поражение мозга не является системным и не ограничивается подкорковыми узлами. Процесс распространяется на различные отделы нервной системы, но изменения в области лентикулярных ядер являются наиболее выраженными и постоянными.
Поражение других отделов имеет следующую последовательность: хвостатое тело, наружный членик бледного шара, глубокие слои мозговой коры, зубчатые ядра мозжечка, ядра гипоталамической области. Остальные отделы мозга поражаются меньше.
Ангиотоксические изменения стоят на первом плане. Они выражаются атонией сосудов, особенно мелких, их расширением, переполнением кровью, образованием стазов, но без развития тромбозов. В различных отделах мозга наблюдаются кровоизлияния. Отмечаются также изменения стенок сосудов с размножением клеток адвентиции и эндотелия, отложением липоидов, гиалинозом капилляров. Вследствие повышенной проницаемости сосудов развивается периваскулярный отёк и аноксическое разрушение нервной ткани. Богатые капиллярами участки мозга поражаются больше всего. Распространение этих изменений в головном мозгу иногда очень обширно, а их характер лучше всего согласуется с представлением о токсическом воздействии крови на сосудистую стенку.
Цитологические изменения выражаются дегенерацией ганглиозных нервных и макроглиальных клеток. Для гепатолентикулярной дегенерации характерно изменение глии (глия Альцгеймера). Глия Альцгеймера образуется из обычных астроцитов, которые бывают двух типов. К первому типу относятся громадные глиозные клетки с бледной протоплазмой и большим, богатым хроматином ядром. Клетки со сморщенным, пикнотическим ядром называют клетками Опальского. Ко второму типу клеток Альцгеймера относятся гигантские ядра, лишенные протоплазмы, которые на окрашенных тионином препаратах представляются «голыми».
Клетки Альцгеймера встречаются в различных отделах мозга, чаще всего в подкорковых узлах, зрительном бугре, гипоталамической области, зубчатом ядре мозжечка. Ганглиозные нервные клетки подвергаются такого же рода изменениям, что и астроциты, которые превращаются в элементы второго типа Альцгеймера.
В печени и извитых канальцах почек обнаруживаются изменения клеток, сходные с альцгеймеровскими. Наблюдаются также нервные клетки с хромолизом в различных стадиях «хронического заболевания» Ниссля (расплавление нервных клеток), реже поражение клеток, определяемых как «тяжёлое» и «отёчное». Воспалительные изменения не выражены. В основе клеточных изменений лежит нарушение клеточного обмена нуклеиновых кислот. Зёрна меди удается обнаружить в различных отделах мозга, больше всего в подкорковых узлах, в наиболее грубо измененных клетках внутри и межклеточно.
Первично страдает печень, изменения в мозгу обусловлены поражением печени. Клинически заболевание печени предшествует неврологическим симптомам.