Цепная реакция. как работают тесты на коронавирус?
Содержание:
Новое открытие
В 70-х годах двадцатого века были открыты ферменты, расщепляющие ДНК в специфических точках. Исследователи получили возможность «разрезать» ДНК на более короткие и стабильные фрагменты.
После этого последовало новое открытие: ученые «научили» ДНК копировать саму себя и достраивать до таких размеров, которые легко опознать. Фактически это позволило идентифицировать по выделенному фрагменту ДНК любой интересующий объект:
- вот — ДНК возбудителя насморка,
- это — стафилококка,
- это — вируса герпеса.
В качестве материала для анализа можно использовать:
- пробу ткани пациента,
- одиночный человеческий волос,
- каплю засохшей крови (обнаруженную на месте преступления),
- мозг мумии.
Даже тело мамонта, пролежавшего 40 тыл. лет в вечной мерзлоте, сможет рассказать, чем болел доисторический гигант.
Все больше и больше специалистов рекомендуют ПЦР-диагностику вместо обычных бактериологических анализов. В первую очередь это урологи и гинекологи — в их сфере плюсы метода ценятся особенно высоко.
Быстро и с гарантией выявляются все зловредные возбудители урогенитальных инфекций:
- хламидиоза,
- уреаплазмоза,
- гонореи,
- герпеса,
- гарднереллеза,
- микоплазменной инфекции и др.
Взяли на вооружение новый метод и пульмонологи (врачи, которые занимаются заболеваниями легких), ведь он позволяет различать вирусные и бактериальные пневмонии, туберкулез. В гематологии ДНК-диагностика выявляет цитомегаловирусы, онковирусы. Ну и, конечно же, не остались в стороне врачи-инфекционисты:
ПЦР используется в качестве экспресс-метода диагностики:
- сальмонеллеза,
- дифтерии,
- вирусных гепатитов В, С и G.
ПЦР-диагностика: много плюсов и один большой минус
Преимущества метода:
— Возбудитель выявляется непосредственно, по специфическому участку ДНК, в отличие от иммуноферментного анализа, при котором вредный микроб выявляется косвенно (по особым белкам — продуктам его жизнедеятельности).
— Возможна четкая идентификация ДНК одного определенного возбудителя. Метод позволяет не спутать его ни с каким другим, как это бывает в том же иммуноферментном анализе, где антигены нескольких микроорганизмов нередко реагируют перекрестно.
— Метод может выявить даже одну-единственную болезнетворную бактерию среди миллиардов других и через несколько часов предоставить 50 миллиардов ее копий! То есть он работает там, где другие методы (микроскопический, бактериологический, иммуноферментный) пасуют.
— Метод универсален. Ведь все на свете ДНК состоят из тех же четырех нуклеотидов:
- аденина (А),
- гуанина (Г),
- цитозина (Ц),
- тимина (Т).
Поэтому способ применим абсолютно для любых бактерий и вирусов. Причем обнаружить можно не только кого угодно, но и где угодно в:
- крови,
- моче,
- мокроте,
- биоптате (маленький кусочек ткани),
- почве.
Результаты анализа можно получить чрезвычайно быстро, ведь возбудителя не надо выращивать искусственно (именно эта процедура при лабораторном исследовании занимает много времени). Ответ, как правило, готов уже через 3-4 часа после обращения.
Один недостаток — сверхчувствительность
Как это часто бывает, достоинства метода иногда становятся и его недостатками. Речь идет о феноменальной чувствительности ПЦР, которая может оборачиваться «ложноположительными» результатами, если в посуде, пипетках и прочем оборудовании для анализа будет хотя бы крошечное количество «чужеродной» ДНК. ПЦР размножит эту ДНК и выдаст неправильный результат.
Но эта проблема решаема — посуда и материалы должны быть одноразовыми, а амплификацию (многократное копирование) ДНК необходимо проводить в отдельном от подготовки проб помещении. Именно поэтому доверять результатам ПЦР-диагностики можно, если вы обратились в солидную лабораторию, оснащенную по последнему слову техники.
Встройте «Правду.Ру» в свой информационный поток, если хотите получать оперативные комментарии и новости:
Подпишитесь на наш канал в или в
Добавьте «Правду.Ру» в свои источники в Яндекс.Новости или News.Google
Также будем рады вам в наших сообществах во , Фейсбуке, Твиттере, Одноклассниках…
Проведение реакции
ПЦР проводят в буферно-солевом растворе с определенным значением рН, содержащем необходимую концентрацию ионов магния, четыре вида дезоксирибонуклеозидтрифосфатов и термостабильную Taq-полимеразу (ДНК-полимераза ряда микроорганизмов, например, Termus aquaticus обладает уникальным свойством сохранять активность при температуре 95°С). Состав буферного раствора, концентрацию реагентов, приготовление растворов указывают в фармакопейной статье и нормативной документации или приводят ссылку на инструкцию по применению набора реагентов для ПЦР. Реакция инициируется парой праймеров, каждый из которых представляет собой последовательность из 20-25 нуклеотидов, один праймер комплементарен последовательности ДНК с 5’-конца амплифицируемого участка, а другой – с 3’-конца. Последовательность праймеров, их концентрацию указывают в фармакопейной статье и нормативной документации.
Для оценки эффективности амплификации следует использовать положительные и отрицательные стандартные и/или контрольные образцы, указанные в фармакопейной статье и нормативной документации или в инструкции по применению набора реагентов.
ПЦР осуществляют в автоматическом режиме на специальных программируемых приборах – амплификаторах, контролирующих заданные параметры реакции: температуру и длительность отдельных этапов цикла (денатурация, гибридизация и синтез цепи ДНК), число циклов и т.д.
Денатурация. Выдерживание при температуре от 94 до 96 °С в течение установленного времени; при этом двойная цепь денатурируется (расплетается) с образованием двух одноцепочечных молекул ДНК.
Гибридизация (отжиг). При температуре 45 – 65 °С в течение установленного времени происходит гибридизация праймеров и одноцепочечной ДНК-матрицы, в процессе которого праймеры распознают комплементарные им участки матричной ДНК.
Синтез цепи ДНК (элонгация). При температуре 65 — 72 °С в течение установленного времени происходит репликация (достраивание) одной из одноцепочечных ДНК от точки связывания праймера «вправо» (для одной цепи ДНК) и «влево» (для другой цепи ДНК). В результате вновь синтезируемые молекулы ДНК становятся, в свою очередь, матрицей для аналогичного синтеза новых копий.
Продолжительность цикла составляет 0,5 — 5 мин. Сразу после окончания первого цикла процедура повторяется и происходит экспоненциальное увеличение содержания фрагментов ДНК. Обычно ПЦР состоит из 25-40 циклов. В каждом цикле происходит удвоение числа копий амплифицируемого участка ДНК, приводящее к увеличению в геометрической прогрессии общего содержания продуктов реакции.
Эффективность ПЦР и количество синтезированного при этом заданного фрагмента ДНК зависит от многих факторов, среди которых следует выделить: тип и термопроводящие характеристики амплификатора, тип используемой ДНК-полимеразы, состав буферного раствора, объем реакционной смеси; длину и первичную структуру праймеров; выбранную специфическую последовательность ДНК.
Используемое оборудование и режим амплификации указывают в фармакопейной статье и нормативной документации или приводят ссылку на инструкцию по применению набора реагентов для ПЦР.
Как происходит сдача анализов на ПЦР
В зависимости от материала, который забирается для проведения анализа ПЦР, существует несколько обязательных правил для пациента. Кровь сдается строго натощак утром. Мочу тоже стоит сдавать утром, первую порцию. Мокрота также сдается натощак, хотя это и необязательно. Мазки сдаются в любое время суток и имеют специфические требования. Мазок из ротоглотки также следует сдавать утром до приема пищи.
Забор материала производится сертифицированным специалистом стерильными одноразовыми инструментами. Берут анализ крови на ПЦР одноразовым стерильным шприцом, из вены забирают приблизительно 1-2 мл венозной крови для выявления таких инфекций как герпес или ВПЧ (вирус папилломы человека). Мочи достаточно 10 мл, мокроты – субстанции, размером со спичечную головку.
Для каждого вида анализа ПЦР существуют свои требования:
- кровь, как говорилось выше, забирают из вены натощак;
- мочу следует сдавать утром, первую порцию. Но, если забор является срочным, то достаточно сдать мочу по прошествии 2 часов после последнего мочеиспускания. Это позволит инфекции набрать необходимую критическую массу на 1 мл для более простого обнаружения патогена;
- как берут соскоб из уретры. Первым делом обрабатывают раствором NaCl 0.9% наружное отверстие уретры. Затем, совершая циркулярные движения, зонд проводят на 2-4 см в уретру. Головку зонда, которая имеет щетинистое строение отсекают и кладут в пробирку со специальным раствором (своеобразный питательный агар для бактерий);
- из влагалища производят мазок. Предварительно убирают секрет бартолиновых желез, затем из заднего нижнего свода влагалища специальной ватной палочкой происходит забор материала. При видимых патологических изменениях во влагалище мазок следует брать непосредственно на поврежденном участке;
- как проводят соскоб из цервикального канала у женщин. Удалив слизь из наружных половых путей, зонд на 0,5 – 1,5 см вводят в шейку матки, совершают циркулярное движение и, не касаясь стенок влагалища, удаляют зонд из половых путей. Затем совершают действия, аналогичные соскобу из уретры;
- из ротоглотки забор происходит натощак. Придерживая кончик языка, зондом производят мазок с задней стенки глотки, по миндалинам или по небным дужкам. Не соприкасаясь со слизистой ротовой полости и зубами, зонд выводится и отправляется на пцр-исследование;
- из конъюнктивы, предварительно очистив физиологическим раствором гнойные выделения, производят соскоб слизистой нижнего века от латерального к медиальному краю. Веко при этом придерживается медицинским работником во избежание соприкосновения зонда со слизистой глаза и ресницами.
Правила подготовки для женщин и мужчин
Правила подготовки для женщин и мужчин
Достоверную информацию о наличии или отсутствии заболевания можно узнать, если соблюдать все правила подготовки к анализу. ПЦР мазок для анализа делают мужчинам и женщинам по направлению акушера, гинеколога или уролога. Материалом в данном случае служит соскоб из влагалища или уретры. В зависимости от целей диагностики на исследование забирают кровь, слюну или сперму.
Подготовка к сдаче ПЦР у мужчин и женщин во многом имеет общие черты, а также свои особенности:
- минимум за 30 дней до сдачи анализа следует прекратить приём любых препаратов, влияющих на результат (антибиотики, противовирусные, противогрибковые, противопротозойные, иммуномодуляторы)
- женщине записаться на приём к врачу нужно после месячных, не раньше, чем через 4-5 дней после последней менструации. Иногда возникают ситуации, при которых возникает вопрос: «Можно ли сдавать мазок во время месячных?». Гинекологи настоятельно не рекомендуют этого делать, чтобы избежать возможной инфекции и получить максимально точный результат;
- за два дня до процедуры следует сохранять половой покой
- подготовка к ПЦР начинается уже накануне — вечером необходимо принять ванну. Утром перед процедурой пользоваться душем нельзя, это снизит эффективность диагностических мероприятий.
- последнее мочеиспускание должно быть минимум за 2- 2.5 часа перед процедурой
- при сдаче крови запрещено употреблять пищу и пить жидкость
При соблюдении этих простых правил полученные мазки для ПЦР-исследования будут максимально информативными, и вам не придётся сдавать их вновь.
Показания к ПЦР

ПЦР на половые инфекции выполняются пациентам, которые:
- жалуются на симптомы со стороны урогенитального тракта;
- вступали в половые контакты с потенциальным или установленным источником венерических инфекций;
- желают обследоваться с профилактической целью (для раннего выявления и лечения венерических заболеваний до возникновения осложнений);
- обследуются по поводу бесплодия;
- планируют лечение бесплодия, в частности с использованием вспомогательных репродуктивных технологий;
- планируют операции на репродуктивных органах (все венерические болезни должны быть выявлены и пролечены для снижения риска инфекционных осложнений).
Как мы уже выяснили, ПЦР выполняется не только для первичной диагностики.
Поэтому показаниями для получения результатов этого исследования также являются:
- прохождение курса терапии по поводу венерического заболевания;
- ВИЧ-позитивный статус (исследования проводятся регулярно для оценки последствий заболевания, особенностей его течения, назначения и коррекции антиретровирусной терапии);
- наличие папиллом на половых органах (для оценки риска рака);
- выявление ЗППП другими методами, например с помощью микроскопии или бак посева (показано обследование методом ПЦР на сопутствующие инфекции).
Нередко ПЦР делают пациентам в случае неудач в лечении тех или иных заболеваний.
Например, если терапия кандидоза не приносит успеха, необходимо исследование для определения вида грибка.
Исходя из этой информации, врач сможет подобрать более эффективную схему медикаментозной терапии.
Анализ методом ПЦР
ПЦР анализ — что это такое? Это метод использует принципы молекулярной биологии. Для исследования материала применяются особые ферменты, которые многократно и быстро копируют ДНК, РНК фрагменты возбудителей болезни. Существует разные виды ПЦР анализа в зависимости от исследуемого материала (кровь, моча, кал и т.д.). После обработки сотрудники лаборатории сравнивают с базой данных полученный результат, выявляют концентрацию, тип возбудителя.
Анализ на ПЦР помещают в специальный амплификатор (прибор), который нагревает и охлаждает пробирки с биоматериалом. Изменения температуры нужны для репликации фрагментов. Точность результата будет зависеть от точности температурного режима. Метод полимеразной цепной реакции помогает выявить:
- инфекционный мононуклеоз;
- ВИЧ;
- цитомегаловирусную инфекцию;
- вирусные гепатиты G, C, B, A;
- инфекции/заболевания, передающиеся половым путем (ИППП/ЗППП): гарднереллез, трихомониаз, уреаплазмоз;
- герпетическую инфекцию;
- онкогенные вирусы;
- листериоз;
- хеликобактерную инфекцию;
- клещевой энцефалит, боррелиоз;
- туберкулез;
- кандидоз.
Крови
На данный момент из-за новизны технологии анализ крови методом ПЦР все еще имеет высокую цену. Для подготовки биоматериала не нужно соблюдать определенные требования. Даже вызванные физическими нагрузками, стрессами, сменой рациона питания изменения состава не влияют на результат исследования. ПЦР анализ крови может испортить только прием антибактериальных средств, поэтому перед сдачей необходимо выдержать паузу между лечением и тестом.
ПЦР исследование крови – самый распространенный вариант диагностики хронических, острых инфекционных патологий при вирусном или атипичном проявлении. Серологические методы исследования имеют определенную трудность при проведении – определение наличия возбудителя проводится по наличию антител в организме человека. Результат мог быть ложноотрицательным, если состояние больного не давало время для их выработки.
Мазка
В сфере гинекологии для исследования наличия инфекционных микроорганизмов используют ПЦР анализ мазка. Работа с материалом проводится по тому же принципу, что и с кровью: многократное увеличение фрагментов ДНК возбудителя, чтобы с легкостью его идентифицировать. Это же помогает обнаружить скрытые инфекции у женщины. Для проведения анализа могут быть взяты разные биологические жидкости: слюна, мокрота, моча, кровь. В гинекологии для точности определения чаще используется мазок со слизистой влагалища из цервикального канала.
Для проведения ПЦР существуют определенные показания. Нередко его нужно сделать, чтобы выявить устойчивый к антибиотикам вид возбудителя. У женщин основными показаниями для диагностики по этому методу выступают:
- беременность, которая протекает тяжело;
- острая фаза ИППП;
- если есть подозрение на переход ИППП в хроническую стадию;
- поиск причин бесплодия.
Кала
Для выявления инфекции может быть назначен со стороны врача анализ кала на ПЦР. Для того, чтобы получить максимально достоверные результаты после теста, необходимо придерживаться следующих правил перед забором биоматериала:
- за несколько суток прекратить прием слабительных препаратов: масла, свечи;
- исключить медикаменты, которые дают специфическую окраску калу, к примеру, с содержанием железа.
Для забора следует использовать стерильную палочку и контейнер. Чем-либо их дополнительно протирать, ополаскивать не нужно. При сборе материала будьте осторожны, вы не должны задеть рукой внутренние стенки контейнера. Следите, чтобы в кале не было примесей мочи, нельзя использовать дополнительные вспомогательные средства для испражнения (клизма). Собирать материал нужно в день сдачи, хватит 1/3 объема контейнера. Данный метод диагностики имеет следующие преимущества:
- Анализ способен указывать на ДНК паразита, другие же тесты могут определять только остатки их жизнедеятельности.
- Высокая точность, будет установлен возбудитель.
- Ультрачувствительный анализ, который способен выявить даже одну клетку вируса.
- Результат исследования ПЦР будет готов через 4-5 часов.
Мочи
При необходимости для проведения теста врач может взять для исследования мочу. Высокая точность открывает возможность работать с любой биологической жидкостью, из которой удается извлечь ДНК вируса. Чтобы сдать анализ мочи ПЦР, нужно придерживаться таких ограничений перед забором материала:
- минимум за 1 день до процедуры прекратить половые контакты;
- за 3 недели до сдачи должно быть окончено любое антибактериальное лечение, потому что медикаменты смажут картину;
- сдавать анализ нужно натощак (жидкость тоже запрещена);
- брать нужно первую утреннюю порцию материала.
Микроскопия мазка
Микроскопия мазка — исследование, направленное на анализ выделений из уретры, влагалища и цервикального канала, проводящееся под микроскопом. Микроскопия мазка наиболее широко распространена в гинекологии, поскольку берется у пациентки каждый прием. Исследование оценивает состояние микрофлоры в вышеперечисленных зонах и степень чистоты влагалища. Оценивается соотношение элементов клеток, наличие патогенных микроорганизмов в той или иной степени, возбудителей, а также признаки возможных воспалительных процессов и инфекций.
Мазок берется с помощью обработанных предметных стекол, разделенных на три части: для мазка из уретры, влагалища и шейки матки соответственно. Каждый сегмент промаркирован соответствующим буквенным обозначением.
Перед отправкой в лабораторию мазки высушиваются на открытом воздухе. Некоторые исследования (например, биопсия) не могут быть совершены без получения данных о состоянии микрофлоры и степени чистоты влагалища.
Комментарии и ссылки
- абы Mullis, Kary (1998). Dancing Naked in the Mind Field. New York: Pantheon Books. ISBN 0-679-44255-3.
- Rabinow, Paul (1996). Making PCR: A Story of Biotechnology. Chicago: University of Chicago Press. ISBN 0-226-70146-8.
- Mullis KB. The unusual origin of the polymerase chain reaction. Sci Am 1990; 262 (4): 56-61, 64-5.
- Advice on How to Survive the Taq Wars 2: GEN Genetic Engineering News Biobusiness Channel: Article. May января 2006
- Отжиг (англ. Annealing) — гибридизация фрагментов ДНК
- Шпилька — внутримолекулярная самокомплементарна структура
- Диммеры праймеров — межмолекулярные структуры, образующиеся праймерами друг с другом или с самим собой
Разновидности ПЦР-анализов
Вариаций такой ПЦР диагностики существует много. Выбор определенного метода зависит от многих факторов: предположительного диагноза, возможностей доступных лабораторий, метода взятия материала и пр.
Наиболее часто используются такие разновидности ПЦР:
- вложенная;
- ступенчатая;
- с горячим стартом;
- виртуальная;
- ассиметричная;
- в реальном времени и т. д.
Преимущественно используют ПЦР в реальном времени, так как способ характеризуется самыми точными результатами и максимальной скоростью обработки данных. После его применения заключение готово через час-два.
Если врач выдает направление на обследование с применением полимеразной цепной реакции, то он должен уточнить, какой именно биоматериал необходимо предоставить пациенту и каким образом подготовиться к отбору пробы.
Анализ крови
Кровь в качестве биоматериала для тестирования берут при подозрении на ВИЧ, вирусный гепатит, токсоплазмы, половой герпес и цитомегалию. Для большинства этих патогенов до использования этого метода диагностика базировалась на выявлении антител к возбудителю, что сильно затягивало время обнаружения микробов в тот период, когда антитела еще не вырабатываются.
Перед сдачей крови для диагностики в данном случае не нужны особые приготовления, но лучше, если проба будет отобрана натощак. Единственное обстоятельство, способное серьезно исказить результаты — прием антибиотиков, поэтому сдаче должен предшествовать временной отрезок после приема подобных лекарств в несколько дней или недель в зависимости от типа антибиотика.
В самых современных клиниках в последнее время для отбора крови на ПЦР используют вакуумные системы, которые минимально повреждают кожные покровы и сводят к минимуму вероятность попадания в пробу загрязняющих агентов из воздуха, инструментов или рук лаборантов.
Анализ мазка
Используется как в гинекологии, так и в венерологии для определения заболеваний, передающихся половым путем. Часто назначают ПЦР мазка во время беременности для выявления скрытых факторов, способных негативно повлиять на формирование плода или ход беременности.
Подготовка к отбору материала заключается в том, чтобы полностью исключить половые контакты за несколько суток до процедуры. Проводить спринцевания марганцовкой или настоями трав тоже нельзя. На протяжении критических дней и 2-х дней после них мазок на ПЦР-анализ не берется.
Отбор биоматериала производят в лаборатории из влагалища, шейки матки, цервикального канала или уретры.
ПЦР-анализ мазка позволяет выявить патоген, который устойчив к определенному виду антибиотиков. Кроме того, показаниями к такому виду диагностического обследования выступают:
- осложненная беременность без видимых причин;
- острое течение венерической болезни;
- предположительное хроническое течение венерического заболевания;
- выявление причин бесплодия или самопроизвольных абортов.
Анализ кала
Анализ кала с применением полимеразной цепной реакции назначается специалистом для уточнения наличия инфекции. Подготовка к отбору пробы кала для ПЦР заключается в следующем:
- исключить за несколько суток слабительные средства в виде любых свечей, масел или оральных медикаментов;
- не употреблять накануне лекарства или продукты, которые придают калу выраженную окраску.
Материал для ПЦР-определения лучше всего доставить в специальном контейнере для кала с палочкой. Внутреннее пространство контейнера стерильно, поэтому протирать или промывать его не следует
Во время отбора образца важно отслеживать, чтобы не задеть внутреннюю поверхность приемника, также в пробе не должно быть следов мочи. Перед отбором запрещено применение клизм
Анализ мочи
Такое исследование с помощью ПЦР позволяет извлечь ДНК образец вируса или бактерии. Забор мочи лучше проводить утром натощак. Лучше всего, если это будет происходить непосредственно в лаборатории.
Обязательные условия подготовки для получения результатов исследования мочи в лаборатории полимеразной цепной реакции:
- выдержать 3 недели после приема антибиотиков;
- перед отбором жидкости не пить и не есть;
- запрет вагинального секса за сутки до сдачи пробы;
- в контейнер нужно поместить первую порцию материала после пробуждения.
Ход реакции
Фотография геля, содержащего маркерную ДНК (первый и последний слоты) и продукты ПЦР
Обычно при проведении ПЦР выполняется 20—35 циклов, каждый из которых состоит из трёх стадий (рис. 2).
Денатурация
Двухцепочечную ДНК-матрицу нагревают до 94—96 °C (или до 98 °C, если используется особенно термостабильная полимераза) на 0,5—2 мин, чтобы цепи ДНК разошлись. Эта стадия называется плавлением (денатурацией), так как разрушаются водородные связи между двумя цепями ДНК. Обычно перед первым циклом проводят длительный прогрев реакционной смеси в течение 2—5 мин для полной денатурации матрицы и праймеров.
Отжиг
Когда цепи разошлись, температуру понижают, чтобы праймеры могли связаться с одноцепочечной матрицей. Эта стадия называется отжигом. Температура отжига зависит от состава праймеров и обычно выбирается на 5 градусов меньше, чем температура плавления праймеров. Неправильный выбор температуры отжига приводит либо к плохому связыванию праймеров с матрицей (при завышенной температуре), либо к связыванию в неверном месте и появлению неспецифических продуктов (при заниженной температуре). Время стадии отжига — 30 сек, одновременно, за это время полимераза уже успевает синтезировать несколько сотен нуклеотидов. Поэтому рекомендуется подбирать праймеры с температурой плавления выше 60 °C и проводить отжиг и элонгацию одновременно, при 60—72 °C.
Элонгация
ДНК-полимераза реплицирует матричную цепь, используя праймер в качестве затравки. Это — стадия элонгации. Полимераза начинает синтез второй цепи от 3′-конца праймера, который связался с матрицей, и движется вдоль матрицы, синтезируя новую цепь в направлении от 5′- к 3′-концу. Температура элонгации зависит от полимеразы. Часто используемые полимеразы Taq и Pfu наиболее активны при 72 °C. Время элонгации зависит как от типа ДНК-полимеразы, так и от длины амплифицируемого фрагмента. Обычно время элонгации принимают равным одной минуте на каждую тысячу пар оснований. После окончания всех циклов часто проводят дополнительную стадию финальной элонгации, чтобы достроить все одноцепочечные фрагменты. Эта стадия длится 7—10 мин.
Количество специфического продукта реакции (ограниченного праймерами) теоретически возрастает пропорционально 2n — 2n, где n — число циклов реакции. На самом деле эффективность каждого цикла может быть меньше 100 %, поэтому в действительности P ~ (1+E)n, где P — количество продукта, Е — средняя эффективность цикла.
Число «длинных» копий ДНК тоже растет, но линейно, поэтому в продуктах реакции доминирует специфический фрагмент.
Рост требуемого продукта в геометрической прогрессии ограничен количеством реагентов, присутствием ингибиторов, образованием побочных продуктов. На последних циклах реакции рост замедляется, это называют «эффектом плато».
2.3 Основные принципы подбора праймеров
При создании ПЦР-тест-системы одной из основных задач является правильный подбор праймеров, которые должны отвечать ряду критериев:
1. Праймеры должны быть специфичны
Особое внимание уделяют 3’-концам праймеров, т.к именно с них начинает достраивать комплементарную цепь ДНК Taq-полимераза. Если их специфичность недостаточна, то, вероятно, что в пробирке с реакционной смесью будут происходить нежелательные процессы, а именно, синтез неспецифической ДНК (коротких или длинных фрагментов)
Она видна на электрофорезе в виде тяжелых или легких дополнительных полос. Это мешает оценке результатов реакции, т.к легко перепутать специфический продукт амплификации с синтезированной посторонней ДНК. Часть праймеров и дНТФ расходуется на синтез неспецифической ДНК, что приводит к значительной потере чувствительности.
2. Праймеры не должны образовывать димеры и петли, т.е. не должно образовываться устойчивых двойных цепей в результате отжига праймеров самих на себя или друг с другом.
Классификация используемых флуорофоров[править | править код]
Специфическое определение: флуоресцентный репортерный зондправить | править код
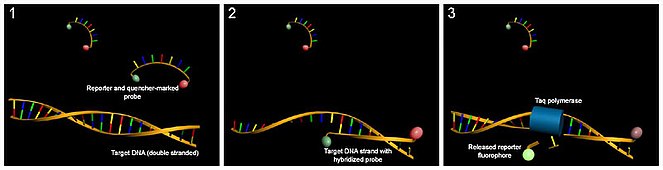
кПЦР с использованием флуоресцентного зонда
Флуоресцентные зонды обнаруживают только ДНК-содержащую последовательность, комплементарную зонду; следовательно, использование репортерного зонда значительно повышает специфичность и позволяет повысить точность измерения в присутствии других дцДНК. Однако флуоресцентные репортерные зонды не предотвращают ингибирующий эффект димеров праймера, которые могут подавлять накопление целевых продуктов реакции.
Можно также использовать несколько зондов, у которых флюорофоры имеют разные спектры испускания. В таком случае появляется возможность в одной пробирке зарегистрировать сигнал от разных молекул ДНК. Метод носит название множественной ПЦР (англ. multiplex PCR).
Метод основан на введении комплементарного продукту амплификации ДНК-зонда с флуоресцентным репортером на одном конце зонда и гасителем флуоресценции на противоположном. Когда гаситель находится в непосредственной близости от репортера, он поглощает сигнал и репортер не даёт флуоресценции. Во время амплификации целостность зонда нарушается и репортер можно обнаружить по флуоресценции после возбуждения лазером. Следовательно, увеличение количества продукта, с которым связывается репортерный зонд в каждом цикле ПЦР, вызывает пропорциональное увеличение флуоресценции. Метки могут флуорессцировать в фазе элонгации или в фазе отжига ПЦР.
Метки, работающие в фазе элонгации:
На зонд с 5’ и 3’ концов пришиты флуорофор и его гаситель. Если последовательность зонда не очень длинная, то даже в связанном с ДНК состоянии они будут взаимодействовать друг с другом, и не будет испускаться флуоресценция. Во время элонгации ДНК-полимераза, обладающая 5’-3’-экзонуклеазной активностью (часто используется Taq-полимераза), по одному нуклеотиду диссоциирует зонд от ДНК-мишени. В результате этого процесса и флюорофор, и его гаситель попадут в раствор, где вероятность нахождения этих веществ рядом будет небольшой, и флуоресценция восстановится.
Метки, работающие в фазу отжига:
- Флуорогенная шпилька — небольшая одноцепочечная молекула ДНК, которая в свободном состоянии способна образовывать особую пространственную структуру ДНК — шпильку. На один конец цепочки пришивают флуорофор, а на второй — вещество, его гасящее. Последовательность зонда комплементарна ДНК-мишени. В таком случае те молекулы зонда, которые плавают в растворе, не будут давать флуоресцентный сигнал, а связавшиеся с молекулами ДНК будут претерпевать конформационные изменения, в результате которых произойдёт пространственное разнесение флуорофор]а и его гасителя и восстановление флуоресценции. Регистрацию целесообразно проводить после денатурации.
- Метка, основанная на методе FRET. Основа этого метода — наличие двух зондов, которые связываются с ДНК-мишенью на небольшом расстоянии друг от друга. На 5’-конец одного зонда и 3’-конец второго пришиты флюорофор-донор и флюорофор -акцептор, соответственно. При их близком расположении флюорофор-донор поглощает свет определённой длины волны и испускает свечение в более длинноволновом спектре. Эту волну, в свою очередь, поглощает флюорофор-акцептор и испускает регистрируемый свет..